Các bảng tổng hợp các thuốc chống động kinh ứng dụng trong lâm sàng
Bảng 13. Các thuốc đặc trị động kinh (theo Robert Berkow)
| Thuốc | Chỉ định | Liều mỗi ngày | Mức thuốc trong máu | Độc tính | ||
| Trẻ em | Người lớn | Điều trị | Độc | |||
| Ethosuximid
(5) |
Cơn động kinh nhỏ | – Dưới 6 tuổi: 0,5g hai lần/ngày. – Trên 6 tuổi: ba lần/ngày. |
0.5g bốn lần/ngày | 40-100
μg/ml |
Trên 100 μg/ml | – Buồn nôn, ngủ lịm, chóng mặt, nhức đầu.
– Đặc ứng: giảm bạch cầu hoặc giảm toàn thể huyết cầu, viêm da, xơ cột bên teo cơ. |
| Trimethadion
(6) |
Như trên (5) | – Dưới 6 tuổi: 0,3g hai lần/ngày.
– Trên 6 tuổi: 0,3g ba lần/ngày. |
0,6g ba lần /ngày. | 15-25
μg/ml |
Trên 25-30 μg/ml | – Chảy mồ hôi, buồn nôn.
– Đặc ứng: quáng gà, giảm bạch cầu trung tính, thiếu máu không tái tạo (aplastic amemia), viêm da, xơ cột bên teo cơ. |
| Clonazepam | Cơn động kinh nhỏ (kể cả không điển hình) rung giật cơ, mất vận động, co cứng trẻ em | Đầu tiên 0,005 – 0,01 mg/kg ba lần/ngày.
Duy trì 0,03 – 0,06 mg/kg ba lần/ngày |
Đầu tiên 0,5 mg ba lần/ngày. Duy trì cho tới 5-7 mg ba lần/ngày | 5-30 μg/ml (mở dấu) | Trên 80 μg/ml | Ngủ gà, mất điều, hành vi bất thường. Hiếm có phản ứng nặng, nhưng trong 1 – 6 tháng có thể giảm dung nạp thuốc hoàn toàn. |
| Valproat | Cơn động kinh nhỏ, rung giật cơ, vàn dộng toàn thân. Màt vận dộng, vận dộng bộ phận. | 15-30 mg/kg (tổng liều tùy cá nhân) ba lần/ngày. Khởi đầu từ từ, đặc biệt nếu trước đó đã dùng thuốc khác | 1-1,5 g/ngày (cách dùng như đối với trẻ em) | Trên 50 μg/ml (trước tiên dùng liều buổi sáng) | Trên
100 μg/ml |
Buồn ngủ và nôn, ngủ gà thoảng qua, giảm bạch cầu trung tính tạm thời |
| Tên thuốc | Dạng thuốc | Thành phần | Liều trung bình ngày | Chỉ định | Tác dụng phụ và đề phòng |
| (1) | (2) | (3) | (4) | (5) | (6) |
| Gardenal | Viên | 0,1g phenobarbital 0,05g phenobarbital 0,01g phenobarbital | 0,10-0,3g | Cơn lớn
Cơn nhỏ Động kinh có ổ |
Buồn ngủ (cho giảm liều) phát ban da (ngừng thuốc rồi dùng lại liều nhỏ hơn) |
| ống tiêm dưới da, bắp thịt | 0,20g phenobarbital 0,04 phenobarbital | 0,20 – 0,40g | Động kinh liên tục | Dùng bơm tiêm thủy tinh sau khi dùng một thuốc tương kỵ bằng bơm tiêm dẻo. | |
| Alepsai | Viên | 0,05g phenobarbital 0,01g Belladone 0,01g cafeine | 0.10 – 0.30g | Như gardenal | Như gardenal |
| Viên | 0,1 Og phenobarbital 0,02g belladon 0,02g cafein | 0,10-0,3g | Như gardenal | Như gardenal | |
| Ortenal | Viên | 0,10g phenobarbital 0,005g phenylaminopropan | 0,10-30g | Như gardenal | Như gardenal |
| Viên nén tác dụng chậm của phenobarbital | Viên | 0,10 phenobarbital | 0,10 – 0.30g | Như gardenal | Như gardenal |
| Aparoxal | Viên E | 0,05g phenobarbital 125mcg sulfate d’ atropine 50mcg hyoscyamin và Scopolamine | 0,10-30g | Như gardenal | Như gardenal |
| Viên A | 0,1 Og phenobarbital 250mcg sulfate d’ atropine 100mcg hyoscyamin và scopolamine | ||||
| Viên M | 0,17g phenobarbital
425mcg sulfate d’ atropin 170mcg hyoscyamin vầ Scopolamine |
||||
| Aparoxal | Giọt | 0,01g phenobarbital 25mcg atropin
10mcg hyosciamin và Scopolamine |
0.10 – 0.30g | Như gardenal | Như gardenal |
| Di -hydan | Viên | 0,10g Diphenylthydantoin | 0,20 – 0,40g | Cơn lớn, dòng kinh có ổ | Buồn nôn, chóng mặt, viêm lợi (giữ vệ sinh miệng), mất điều, hội chứng tiểu não, láy mắt (giảm liều), chống chỉ định với phụ nữ có thai |
| Mysoline | Viên | 0,25g primidon | 0,50 – 2g | Con lớn | Buồn ngủ, chóng mặt, mất điều (giảm liều) |
| Posedrine | Viên | 0,33g beclamid | 1 – 3g | Cơn lớn | |
| Tegretol | Viên
Dịch treo |
– 0,20g carbamazepm
– 5ml; 0.10g carbamazepín |
0,60 – 1,20g | Cơn lớn
Cơn nhỏ Động kinh có ổ |
– Buồn ngủ. chóng mặt, buồn nôn (giảm liều)
– Chống chỉ định với phụ nữ có thai |
| Depakin | Viên Dich treo | – 0,20g Dipropylacetate -1ml: 0,20g Dipropylacetate | 1 – 1,40g | Cơn lớn, cơn nhỏ Động kinh có ổ | Buồn nôn, đau dạ dầy (giảm liều) |
| Viên | 0,30g Dipropylacetamide | 0,90 – 1,80g | Cơn lớn
Động kinh có ổ |
Hen, buồn ngủ (giảm liều) | |
| Depamid | Viên | 0,30g Dipropylacetamide | 0,9 -1,8g | Cơn lớn
Động kinh có ổ |
Hen, buồn ngủ |
| Trinuride | Viên | 0,20g phenetund 0,1 Og Biuret 0,04g phenytoin 0,015g phenobarbital | 3- 5Viên | Cơn lớn Động kinh có ổ | Giảm huyết cầu toàn thể (thường gặp NFS). Viêm gan (thường gặp transaminase). Chống chỉ định: phụ nữ có thai |
| Rivotril | Vién
ống (tĩnh mạch) |
0,002g clonazepam 0,001g clonazepam | 0,006g
0,001g |
Cơn lớn, cơn nhỏ Động kinh liên tục Động kinh có ổ | Hen, buồn ngủ, mất điều (giảm liều) |
| Trimethadion
Abbott |
Viên | 0,30g tnmethadion | 0,30 – 1,20g | Cơn nhỏ | Giảm huyết cầu toàn thể (thường gặp NFS). Ban da, sợ ánh sáng, bệnh thận. |
| 2arontin | Nang
Siro |
0,25g ethosuximid 1mr0,05ethosuximid | 1,0- 1,5g | Cơn nhỏ | Buồn nôn, chóng mặt, đau đầu (giảm liều). Giảm huyết cầu toàn thể (thường gặp NFS). |
| Epiclase | Vìên | 0,30g phenacemid | 1-2g | Động kinh tâm thần vận động | Ban da (giảm liều). Giảm huyết cầu toàn thể, viêm gan, protein niệu. |
| Liều thường dùng mỗi ngày (mg/kg) | Liều thường dùng mỗi ngày (mg) | Số liều tối thiểu mỗi ngày | Thời gian nóng độ thuốc hằng định (ngày) | Nồng độ thuốc tối ưu trong máu (trong 1 ml) | Tác dụng phụ chọn lọc và các phản ứng đặc ứng | |
| A – Cơn lớn hoặc cơn động kinh có ổ | ||||||
| Phenyloin | 4-8 | 200 – 400 | 1 | 5-10 | 10 – 20 mcg | Láy mắt, mất điều, loạn vận ngôn, an thần, lú lẫn. tăng sản ở lợi, rậm lông, thiếu máu hồng cầu khổng lố, loạn tạo máu, ban da, sốt, luput ban đỏ hộ thống, bệnh hạch bạch huyết, bệnh thần kinh ngoại vi, loạn vận động, |
| Carbamazepin | 5-25 | 600- 1200 | 2 | 3-4 | 4 – 8 mcg | Láy mắt, loạn vặn ngôn, nhìn đôi, mất điều thiu ngủ, buồn nôn, loạn tạo máu, độc với gan |
| Phenobarbital | 2-5 | 100 – 200 | 1 | 14-21 | 10 – 40 mcg | Thiu ngủ, lảy mát, mất điều, ban da, kém sáng suốt, tăng vận động. |
| Primidon | 5-20 | 750- 1500 | 3 | 4-7 | 5- 15mcg | An thần, láy mắt, mất điều, buồn nôn, chóng mặt, ban đỏ, thiếu máu hồng cầu khổng lồ, trạng thài kích thích |
| Valproic acid | 10-60 | 3 | 2-4 | 50 – 100 mcg | buồn nôn, nôn, tiêu lỏng, thiu ngủ. rung tốc, tăng cân, đôc gan, giảm tiểu cầu, run. | |
| B – Cơn vắng ý thức (cơn nhỏ) | ||||||
| Ethosuximid | 20-35 | 1000-1500 | 2 | 5-10 | 40- 100 mcg | Buồn nôn, nôn, chán ăn, đau đầu, ngủ lịm, kèm sáng suốt, loạn tạo máu luput ban đỏ hệ thống, mề day, ngứa |
| Clonazepam | 0.05 – 0,2 | 2 | 20 – 80 mcg | Thiu ngủ, mất điều, kích thích, biến đổi nhãn cách, kịch phát cơn co cứng – co giật. | ||
| Valproic acid | (như trên) | |||||
| C- Cơn giật rung cơ | ||||||
| Valproic acid | (như trên) | |||||
| Clonazepam | (như trên) | |||||
Chú thích: Theo Steven A. Schroeder. Curront Medical Diagnosis and Treatment Appleton – Lange, California, Norivalk, 1992, 772 (dẫn tài liệu của Ammoff M.J.).
Cơ chế tác dụng của thuốc chống động kinh
Thuốc được sử dụng trong điều trị động kinh ít nhất từ 2500 năm trước đây, và một số lượng lớn phương thuốc đã được thử nghiệm. Người ta cho rằng hiệu quả điều trị thực sự đầu tiên được thông báo vào ngày 11/5/1857 bởi Sir Charles Locock ở Bệnh viện Royal của London (Anh) và kết quả thành công ở 13 trường hợp động kinh với Bromua. Thuốc này còn giữ tính độc quyền cho đến khi phenobarbital ra đời năm 1912. Năm 1938, một bước đột phá tiếp theo khi phát hiện ra hiệu quả chống co giật của phenytoin. Lennox đã viết: “Sự ra đời của phenytoin là một bước tiến quan trọng trong điều trị động kinh” và sau đó những dẫn chất của phenytoin được gia tăng rất nhanh. Từ đó đến nay, việc nghiên cứu tìm các thuốc chống động kinh hiệu quả hơn, dung nạp tốt hơn vẫn đang được tiếp tục.
Mặc dù cơ chế chống co giật và chống động kinh của hầu hết các thuốc chống động kinh hiện có chưa được xác định rõ, việc tìm hiểu các cơ chế này vẫn là cực kỳ quan trọng.
Một loại thuốc chống động kinh có thể có nhiều tính chất sinh học thần kinh. Một số thuốc tác động theo một phương thức chủ yếu, một số khác có một hoạt tính sinh học phức tạp hơn, có liên quan đến kích cỡ của phổ tác động điều trị. Phương thức tác động đó ảnh hưởng tới các đặc tính của màng nội tế bào thần kinh hoặc tới các chất trung gian dẫn truyền thần kinh.
Nói chung, các thuốc chống động kinh dường như làm giảm tính kích thích neuron hoặc tăng sự ức chế bằng cách thay đổi sự dẫn truyền các ion Na+, K+ hoặc Ca++ hoặc bằng cách tác dụng lên hoạt tính của GABA, glutamat hoặc các chất dẫn truyền trung gian thần kinh khác có liên quan đến hoạt động động kinh. Mặc dù một số thuốc chống động kinh có cơ chế giống nhau, mỗi loại thuốc lại có những cơ chế riêng biệt và nhiều loại thuốc mới có cơ chế tác dụng khác cơ chế của những thuốc đã được khẳng định rõ.
Có 4 phương thức tác động chủ yếu của các thuốc chống động kinh:
+ Ngăn chặn các kênh Na+ phụ thuộc điện thế: natri valproat, phenytoin, carbamazepin, lamotrigin.
+ Ngăn chặn các kênh Ca++ phụ thuộc điện thế: ethosuximid, natri valproat.
+ Tăng cường hoạt động của hệ GABA (gama amino butyric acid); benzodiazepin, phenobarbital, natri valproat. Một số thuốc mới như gabapentin có cấu trúc đồng dạng với GABA bởi tăng cường tổng hợp và giải phóng GABA.
+ Giảm dẫn truyền kích thích của hệ glutamat: phenobarbital.
Sau đây là cơ chế tác dụng của một số thuốc chống động kinh chính:
– Phenytoin: là một thuốc chống động kinh được sử dụng rộng rãi nhất và được nghiên cứu sâu nhất, là một thuốc được ưu tiên dùng cho động kinh co cứng co giật, là một acid hữu cơ yếu, hầu như không tan trong nước. Phenytoin có thể qua màng tế bào, một đặc tính cho phép nó tiếp cận dễ dàng với các vị trí tác dụng nội bào. Hoạt động của thuốc là kết quả của những hoạt động đa dạng.
Tác dụng của phenytoin trên các cơn động kinh do sốc điện cực đại gây ra, đã cung cấp một manh mối quan trọng về cơ chế tác dụng của nó, phenytoin làm mất pha co cứng tăng trương lực của cơn co cứng co giật do điện gây ra. Ở một thử nghiệm khác, người ta áp nhôm hoặc cô ban vào vỏ não gây ra các cơn động kinh cục bộ và tạo ra một mô hình thực nghiệm đối với động kinh cục bộ đơn giản. Sử dụng liều điều trị thông thường của phenytoin làm hạn chế sự phát triển của hoạt tính động kinh tối đa trong các ổ động kinh và giảm sự lan truyền hoạt động động kinh từ ổ động kinh, chứng tỏ rằng phenytoin tác động đến cường độ và sự lan truyền của động kinh mà không tác động đến sự khởi đầu của động kinh và cũng gợi ý rằng phenytoin gây ra một sự ức chế tính tăng kích thích neuron.
Cơ chế tác dụng được nhiều người công nhận là chẹn kênh Na+ phụ thuộc liều của phenytoin. Kênh điện thế Na+ liên quan đến sự phát sinh và dẫn truyền của điện thế và hạn chế tần sô của sự phóng điện neuron. Hậu quả của việc chặn các phóng điện là làm giảm điện thế co giật. Sự lan truyền điện thế kích thích có thể gây ra sự tăng giảm phân cực lan rộng mà làm cơ sở cho sự phóng lực nhọn giữa cơn và tạo điều kiện cho sự lan tỏa của hoạt động động kinh từ các ổ. Do đó, việc ngăn chặn điện thế co giật được coi là cơ chế quan trọng mà phenytoin ngăn cản được cơn động kinh.
Một cơ chế hoạt động khác của phenytoin là sự kích thích hoạt động của Na+ – K+ – ATPase. Ảnh hưởng này xuất hiện mạnh nhất khi K+ ở trong tế bào thấp hơn và Na+ cao hơn mức thông thường. Điều kiện này có thể xảy ra trong những tế bào thần kinh ở ổ động kinh, phenytoin giúp các tế bào thần kinh duy trì được các cân bằng ion bình thường thông qua sự kích thích bơm ion. Đây cũng là hiệu quả quan trọng chống co giật của phenytoin.
Phenytoin cũng làm giảm sự dẫn truyền điện thế liên quan đến hiệu điện thế phụ thuộc Ca++.
Phenytoin làm giảm sự dẫn truyền qua synap. Sự giảm dẫn truyền qua synap có thể bị gây ra bởi sự ức chế cả dòng Na+ và Ca++.
– Valproat: là một trong những thuốc chống động kinh quan trọng nhất trong hai thập kỷ qua, có phổ điều trị rộng trên tât cả các thể động kinh và không gây ngủ. So sánh hiệu quả với phenytoin (đơn liệu pháp) thấy không có sự khác biệt lớn. Đối với cơn vắng điển hình. Valproat và ethosuximid đều có tác dụng tốt, là thuốc được lựa chọn đầu tiên và có thể dùng phối hợp trong trường hợp kháng thuốc. Valproat có lợi thế điều trị cho những bệnh nhân có hai loại cơn động kinh kết hợp (cơn hỗn hợp).
Cấu trúc acid béo phân nhánh khác hẳn với cấu trúc dị vòng của các thuốc chống động kinh cổ điển. Cơ chế tác dụng của thuốc chưa được biết rõ mặc dù đã có rất nhiều giả thiết được đặt ra. Tuy nhiên, có 2 cơ chế chống co giật chính được nhiều người công nhận.
Thứ nhất là thuốc làm tăng hoạt động GABA trong não, ví dụ điều trị với valproat sẽ làm tăng nồng độ GABA lên 30 – 40%. Nhiều cơ chế đã được đê cập để giải thích tăng nồng độ GABA, chủ yếu thông qua con đường ức chế hoặc thúc đẩy chuyển hóa bằng cách:
+ Hoạt hóa men glutaminic acid decarboxylase mà enzym này tổng hợp nên GABA từ glutamat.
+ Úc chế men GABA transaminase và succinic semialdehyd dehydrogenase, enzym thứ nhất và thứ hai trong của quá trình thoái biến GABA.
+ Valproat củng có thể tăng cường ức chế tại hậu synap thông qua trung gian GABA như benzodiazepin và barbiturat nhưng chỉ được thấy ở trên vùng điều trị.
Thứ hai, ở mức tế bào, valproat có thể ức chế sự tái phân cực hóa gây ra bởi dòng vào của Na+. Ảnh hưởng trên sự phát xung tế bào dường như giống với phenytoin và carbamazepin, gợi ý một cơ chế tương tự. Trong các nghiên cứu tại đồi hải mã, valproat chặn giữ các hoạt động hình thành cơn động kinh và hoạt hóa sự dẫn truyền Ca++ phụ thuộc K* (Dean, 1997).
- Carbamazepin: có hiệu quả lâm sàng và thực nghiệm tương tự như phenytoin. Ở mức độ tế bào với nồng độ điều trị carbamazepin làm hạn chế tần số xuất hiện sự phóng điện của neuron. Giống như phenytoin, carbamazepin phong tỏa kênh Na+ khử cực và làm chậm quá trình tái khử cực. Cũng tương tự như phenytoin, carbamazepin ức chế quá trình đi vào qua màng synap của ion Ca++.
Về mặt cơ chế, carbamazepin liên quan tới các chất chống trầm cảm 3 vòng. Không có bằng chứng nào cho thấy hoạt động chống co giật của carbamazepin lên hệ thống dẫn truyền thần kinh.
- Phenobarbital: thuộc nhóm được sử dụng rộng rãi như là thuốc ngủ, an thần, gây mê. Phenobarbital là một trong số các barbiturat có hiệu quả như là chất chống động kinh ở liều không cao hơn liều an thần. Phenobarbital làm tăng ngưỡng phát sinh co giật và do đó có thể có cơ chế hoạt động khác nhau. Nó tác động tới quá trình khởi động và ức chế các cơn co giật gây ra bởi amygdaloid. Phenobarbital cũng làm phong bế các ổ động kinh và ức chế việc truyền xung động thần kinh tới các vùng vỏ não. Phenobarbital ức chế chọn lọc các hoạt động bất thường mà không phá vỡ sự phát xung điện thông thường.
Cơ chế hoạt động ở mức tế bào của phenobarbital là tăng ảnh hưởng ức chế lên các neuron và làm giảm tác động kích thích. Cả hai ảnh hưởng này có thể quan sát thấy ở liều điều trị do làm tăng có chọn lọc các phản ứng của GABA và làm giảm phản ứng của glutamat. Nghiên cứu cũng chỉ ra rằng phenobarbital ngăn cản dòng Ca++ vào trong synap do sự khử cực, có thể làm giảm sự giải phóng các chất dẫn truyền phụ thuộc vào Ca++.
| Thuốc | Cơ chế tác dụng | |
| Điện sinh lý | Sinh hoá | |
| 1 Phenytoin | Giảm điện thế sau tetani (protentiel post tètanique). Lan toả sự kích hoạt co giật và sự kích thích của dây thần kinh ngoại vi. Làm tăng hoạt động của tế bào Purking. | Làm tăng vận chuyển Na vá nồng dồ glutamin, serotonin và hydroxy adenoin monokali (HAMK). Làm giảm khả năng hấp thu Ca, AMP vòng, HMP vỏng, acid glutamic và giải phóng các chất chuyển vận. |
| 2 Barbiturat | Tăng ngưỡng kích thích điện và hoá học. Giảm biên độ của điện thế tác dụng, lan toả sự kích hoat co giật và sự kích thích của dây thần kinh ngoại vi. | Giảm sự tổng hơp acetylcholin và ATP, sự chuyển hóa năng lượng lượng của não và sự chảy dồn Ca trước synap. |
| 3. Primidon | Tăng ngưỡng kích thích điện và hoá học, giảm sự lan tỏa và hoá học, giảm sự lan toả kích hoạt co giật. | |
| 4. Carbamazepin | Giảm sự dẫn truyền ở nhân trước bụng của đồi thị, tăng ngưỡng kích thích điện. | Giảm xuyên thấm Na (khi nồng độ cao), ức chế sự tích tụ AMP vòng. |
| 5. Succimid | Tăng ngưỡng lên cơn co giật do Pentilentetrazol và sốc diện càm ứng. | Giảm xuyên thấm kali |
| 6. Acid valproic | Giảm sự lan toả kích hoạt co giật. Tàng ngưỡng lên cơn co giật do Bicuculline, Picrotoxin vá Pentilentetrazol cảm ứng. | Tăng nóng độ hydroxy adenosln monokali (HAMK) vầ sự xuyên thấm kali qua màng. Giảm nồng độ succinat và hydroxy monophosphat vòng (HMP vòng) |
| 7. Benzodiazepam | Tăng ngưỡng lên cơn co giật sốc diện va Pentílentetrazol | Giảm xuyên thấm kali. Có tác dụng tương tự như clonazepam và glycin |
| 8 Tnmethadion | Ngăn trở sự lan truyền xung động qua vòng neuron của đồi thị, tăng ngưỡng lên cơn co giât do sốc diện vá Pentilentetrazol | Giảm xuyên thấm kali, tăng sự tích tụ nội tế bào CO; cùng với sự ngắt quãng sự chuyển hoá của tế bào. |
Sự chuyển hóa của các thuốc chống động kinh
Đặc tính hấp thu và chuyển hóa của thuốc chống động kinh
Thuốc chống động kinh thường được sử dụng bằng đường uống. Để có tác dụng, thuốc phải được hấp thu qua hệ thống tiêu hóa, xâm nhập vào vòng tuần hoàn, hòa tan trong dịch não tủy và tác dụng lên các neuron hoặc màng tế bào. Sau khi được hấp thu, một phần thuốc sẽ được gắn kết với protein huyết tương. Thuốc ở dạng gắn kết có tác dụng như một kho dự trữ để duy trì nồng độ thuốc ở dạng tự do một cách ổn định và để kéo dài thời gian tác dụng của thuốc. Tốc độ thuốc vượt qua hàng rào máu não phụ thuộc vào sự có mặt của thuốc ở dạng tự do trong huyết tương. Nhờ nồng độ thuốc ở dạng tự do tạo ra gradien nồng độ mà thuốc vượt qua được hàng rào máu não. Trong thực hành lâm sàng, nồng độ toàn phần của thuốc được coi như tương đương với nồng độ thuốc có trong não.
Ngay khi bắt đầu có sự hấp thu thì cũng bắt đầu quá trình chuyển hóa hóa sinh của thuốc tại gan. Đối với hầu hết các thuốc chống động kinh, tốc độ chuyển hóa hóa sinh tăng tuyến tính với nồng độ thuốc. Mối liên quan này được gọi là dược động học bậc 1 (first order kinetic), trong trường hợp tốc độ chuyển hóa hóa sinh phụ thuộc vào nồng độ thuốc nhưng mối liên quan giữa liều dùng và nồng độ thuốc là không tuyến tính thì mối liên quan này được gọi là dược động học bậc 0 (zero order kinetic).
Trong các thuốc chống động kinh, chỉ có phenytoin là có dược động học không tuyến tính. Điều này là đặc biệt quan trọng đối với việc sử dụng phenytoin. Ở nồng độ thấp, phenytoin chuyên hóa theo kiểu dược động học bậc 1. Nhưng khi nồng độ đạt đến ngưỡng điều trị, hệ thống enzym trở nên bão hòa, hoạt động của các enzym đã đạt đến cực đại, lúc đó sự chuyển hóa thuốc sẽ theo kiểu dược động học bậc 0. Do hệ thống enzym trở nên bão hòa, tốc độ hoạt động không còn tăng được nữa, vì vậy chỉ cần tăng một lượng nhỏ liều cũng gây ra tăng nồng độ trong huyết tương một cách không tương xứng. Trên lâm sàng, trong một số trường hợp khi tăng liều phenytoin có thể dẫn đến việc chuyển nồng độ thuốc từ dưới ngưỡng điều trị tới ngưỡng độc tính.
Nồng độ thuốc
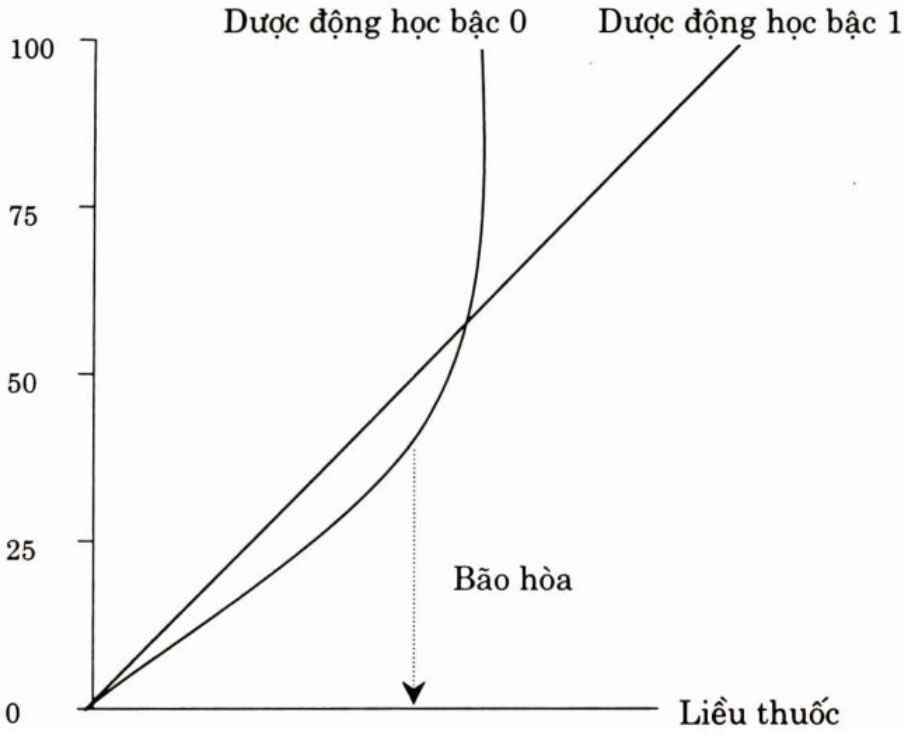
Hình 7: So sánh dược động học bậc 1 và bậc 0.
Trẻ em rất nhạy cảm với ngưỡng độc tính này. Kiểm soát nồng độ phenytoin trong huyết tương là đặc biệt quan trọng và việc tăng liều cần phải được tiến hành từ từ với từng lượng nhỏ một. Printera gợi ý tăng liều 50 mg/ngày nếu nồng độ huyết thanh là nhỏ hơn 12 mg/1 và 30 mg/ngày nếu nồng độ cao hơn.
Thời gian bán hủy của thuốc chống động kinh
Thời gian bán hủy huyết tương của một thuốc là khoảng thời gian cần thiết để nồng độ thuốc trong huyết tương giảm đi một nửa.
Thời điểm sử dụng thuốc tối ưu của bất kỳ loại thuốc nào liên quan đến việc sử dụng thuốc trùng với thời điểm bán hủy sinh học nếu muốn có một hiệu quả thuốc được duy trì ổn định. Mục đích của điều trị là duy trì nồng độ đỉnh của thuốc nam trong khoảng trị liệu và ngăn cản nồng độ đỉnh đạt tới ngưỡng độc tính. Mặc dù các thuốc chống động kinh có thời gian bán hủy rất khác nhau nhưng nhìn chung đối với đa số các bệnh nhân, việc sử dụng thuốc 2 lần/ngày là thuận tiện đối với họ. Với việc uống thuốc nhiều lần trong ngày (> 1 lần) thì pha hấp thu và thải trừ gối lên nhau và sự khác nhau về nồng độ là nhỏ giữa nồng độ đỉnh và nồng độ đáy. Theo Leppik I. (1998), việc điều trị động kinh đòi hỏi nồng độ thuốc ổn định được duy trì ở vị trí thụ cảm thể hoạt động trong suốt thời gian. Không giống như đau hoặc nhiễm khuẩn vì đối với những bệnh này thì việc đạt được một cách ngắt quãng nồng độ thuốc giảm đau hoặc kháng khuẩn là vẫn chấp nhận được, động kinh được kiểm soát tốt nhất khi mà ít có sự biến đổi nhất nếu có thể được về nồng độ thuốc trong suốt thời gian.
Valproat acid (thời gian bán hủy ngắn) cần được sử dụng nhiều lần/ngày. Nhưng nhờ có dạng viên chậm hạn chế sự dao động nồng độ trong huyết tương mà có thể sử dụng 2 lần/ngày. Carbamazepin có khoảng cách giữa liều độc và liều điều trị hẹp nên cần phải sử dụng thuốc sao cho khoảng cách giữa các lần dùng thuốc ngắn hơn thời gian bán hủy của thuốc. Carbamazepin hiện tại cũng đã có dạng phóng thích chậm. Phenobarbital và phenytoin có thời gian bán hủy dài, thuốc vẫn thường được sử dụng 2 lần/ngày mà không gây hậu quả gì.
Bệnh nhân được đưa thuốc bằng đường uống và đưa nhiều lần kế tiếp nhau sau những khoảng thời gian nhất định thì đạt nồng độ ổn định hay giai đoạn bình nguyên của thuốc. Khoảng thời gian này bằng 5 lần thời gian bán hủy của thuốc và tại thời điểm đó, nồng độ thuốc ở trạng thái phân bố ổn định (Css) chỉ còn liên quan đến độ bài xuất (CL) và liều lượng. Bảng 18 cho thấy thời gian để đạt được nồng độ ổn định của một số thuốc chống động kinh.
Bảng 17. Chỉ số dược lý của các thuốc chống động kinh (theo J. Buruni và B.J. Wilder, 1984)
| Thuốc chống động kinh | Hấp thu | Thời gian dạt mứt: tối đa của thuốc trong huyết tương (giờ) | Khối lượng thuốc
khuyếch tán ước định trong cơ thê (i/kg) |
Thời gian giảm 1/2 nồng độ thuốc sau hấp thu và khuyếch tán
(giờ) |
Thời gian đạt trạng thái ổn định (ngày) | Tỷ lệ thuốc cố định và albumin
(%) |
| 1. Phenytoin | Chậm | 8-12 | 0,5-0,8 | 10-40 | 7-9 | 70-95 |
| 2. Primidon | Chậm
vừa |
2-4 | 0,6-0,7 | 6-18 | 4-7 | 0 |
| 3. Phenobarbital | Vừa | 4-7 | 0.7-1,0 | 50-150 | 14-21 | 40-60 |
| 4. Carbamazepin | Chậm
vừa |
6-24 | 0.8-1,4 | 12-35 | 3-4 | 70-80 |
| 5. Ethosuximid | Nhanh | 3-7 | 0,7-0,9 | 20-60 | 7-10 | 0-10 |
| 6. Acid valproic | Nhanh | 1 -4 | 0,15-0,4 | 8-12 | 4 | 90-95 |
| 7. Trimetadion | Nhanh | 1-3 | 0,8 | 14-16 | 30 | 0 |
| 8. Clonazepam | Nhanh | 1-3 | 2,4 | 22-33 | 47 | |
| 9. Metsuccimid | Nhanh | 1-4 | 2-4 | 0-10 | ||
| 10. Diazepam (uống) | Rất
nhanh |
0,5-3 | 1-2 | 27-48 | 4-10 | 90-96 |
Bảng 18. Thời gian bán hủy và thời gian đạt nồng độ ổn định của thuốc chống động kinh (theo Rowan và cs, 1979)
| Thuốc | Thời gian bán hủy | Thời gian đạt nồng độ ổn định |
| Carbamazepin | 12 giờ | 3 ngày |
| Valproat | 12 giờ | 3 ngây |
| Primidon | 12 giờ | 3 ngay |
| Phenytoin | 1 ngày | 5 ngay |
| Ethosuximid | 2 ngày | 10 ngày |
| Phenobarbital | 4 ngày | 3 tuần |
Tương tác thuốc
Vấn đề phối hợp thuốc trong điều trị là một thực tế không thể tránh khỏi và trong nhiều trường hợp lại rất cần thiết. Tương tác thuốc là hiện tượng xảy ra khi nhiều thuốc được sử dụng đồng thời. Sự phối hợp này làm thay đổi tác dụng hoặc độc tính của một trong những thuốc đó.
Trong đa số trường hợp, người thầy thuốc chủ động phối hợp thuốc nhằm lợi dụng tương tác thuốc theo hướng có lợi để tăng hiệu quả điều trị, giảm tác dụng phụ hoặc để giảm độc thuốc. Trong thực tế điều trị có những tình huống hoàn toàn bất ngờ, cùng một thuốc ở mức liều điều trị mà khi phối hợp với thuốc này lại giảm hoặc mất tác dụng, ngược lại dùng với thuốc khác thì xảy ra ngộ độc.
Sự tương tác giữa thuốc chống động kinh với những thuốc khác, đặc biệt là ảnh hưởng của những thuốc khác đến thuốc chống động kinh. Thuốc chống động kinh thường kích thích các thuốc khác, gây nên nồng độ giảm hơn. Sự tương tác rõ rệt xảy ra với thuốc chống đông, thuốc tránh thai, và steroid. Ngược lại, sự ảnh hưởng của những thuốc khác lên thuốc chống động kinh thường là ức chế và có thể gây nên nồng độ độc.
Một dạng khác của tương tác dược động học không liên quan đến hoạt động enzym là thay thế protein huyết tương mà làm tăng các mảnh tự do của thuốc. Các thuốc được vận chuyển trong máu dưới dạng liên kết với protein huyết tương, luôn luôn tồn tại một cân bằng động giữa dạng thuốc tự do và thuốc liên kết. Chỉ có dạng thuốc tự do mới có tác dụng dược lý, còn dạng liên kết giống như một kho dự trữ và nhả dần thuốc ra dạng tự do khi nồng độ thuốc tự do bị giảm.
Bảng 19. Các thuốc tác động đến nồng độ phenytoin trong huyết tương
| Lám tăng nóng độ (a) | Làm giảm nống độ |
| 1. Disultiram | 1. Carbamazepin |
| 2. Sultiam | 2. Ethanol |
| 3. lsoniazid | 3. Acid valproic |
| 4. Dicoumarin | 4. Phenobarbital (b) |
| 5. Phenyramidol | 5. Primidon (b) |
| 6. Phenobarbital | 6. Salicylat (liều cao) |
| 7. Primidon | 7. Acid folic |
| 8. Chloramphenicol | 8. Phenylbutazon |
| 9. Méthylphenydat | 9. Diazepam (b) |
| 10. Sulfamethizol | 10. Chlordiazepoxid (b) |
| 11. Phény!butazol | 11. Clonazepam (b) |
| 12. Sulfaphenazol | |
| 13. Ethosuximid | |
| 14. Chlorpromazin | |
| 15. Prochlorperazin | |
| 16. Propoxyphen |
Chú thích:
(a): Theo thứ tự giảm khả năng xảy ra.
(b): Hiếm gặp trong lâm sàng, còn có những tài liệu mâu thuẫn.
Bảng 20. Các thuốc mà nồng độ trong huyết tương bị giảm do ảnh hưởng của phenytoin
| 1. Digitoxín | 6. Doxycydin |
| 2. Bishydroxycoumarin | 7. Phenylbutazol |
| 3. Méthyrapon | 8. Cortisol |
| 4. Thuốc chống thai loai uống | 9.2.5 – Hydroxycholecalciíerol |
| 5. Dexamethason | 10. Thyroxin |
Nồng độ tự do có thể thay đổi do hậu quả của sự thay thế gắn kết protein bởi thuốc khác, ở trẻ em và người già, phụ nữ trong thời kỳ có thai, và ở bệnh nhân giảm albumin, sự thay thế protein trong huyết tương là liên quan lâm sàng chỉ với thuốc liên kết mạnh.
Ví dụ, mảnh tự do của phenytoin trong huyết thanh bình thường khoảng 10% (0,1), còn lại 90% được liên kết với protein huyết thanh. Vì vậy, ở nồng độ toàn phần 20 mg/1, mức tự do là 2 mg/1. Nếu 5% của nồng độ toàn phần phenytoin bị thay thể bởi sự thêm vào của valproat, mảnh tự do của phenytoin là 0,15 hoặc 15%. ở nồng độ toàn phần phenytoin 20 mg/1, nồng độ tự do là 3,0 mg/1, tương đương mức toàn thể 30 mgA với nồng độ tự do bình thường. Sự tăng lên 50% này có thể gây nên các phản ứng lâm sàng độc tính ở nồng độ toàn phần thường xuyên không phối hợp với hiệu quả như vậy.
Tương tác giữa các thuốc chống động kinh: khi hai hoặc nhiều thuốc chống động kinh được uống cùng một lúc, điều quan trọng là phải xem xét sự tương tác dược động học giữa các thuốc để xác định sự phối hợp thuốc là có hợp lý hay không. Khi hai thuốc được uống cùng một lúc, hiệu quả phối hợp có thể thêm vào (additive) (bằng với tổng số của mỗi hiệu quả riêng biệt), cao hơn nhiều (suppa – additive) (lớn hơn tổng số của mỗi hiệu quả riêng biệt), hoặc thấp (infra – additive) (ít hơn hiệu quả của mỗi thuốc). Hiệu quả cao hơn khi phối hợp thuốc là mỗi thuốc khi dùng đơn độc thì không đủ hiệu quả, vì ràng giới hạn của thuốc chống động kinh ở liều cao hơn lại kèm theo độc tính thần kinh liên quan đến liều. Hơn nữa, sự kiểm soát cơn được bảo đảm bởi sự phối hợp ở liều dung nạp tối đa sẽ không lớn hơn liều dung nạp tối đa của mỗi thuốc khi sử dụng đơn độc. Từ quan điểm trên, sự phối hợp của hai thuốc chống động kinh chỉ có thể là tối ưu khi sự kiểm soát cơn đạt hiệu quả cao và độc tính thần kinh là thấp. Theo Mattson (1997), chỉ có một số ít phối hợp thuốc chống động kinh là đem lại kết quả tối ưu: valproat kết hợp với ethosuximid, valproat và carbamazepin, valproat và phenytoin.
Việc sử dụng kết hợp hai thuốc chống động kinh cũng có thể có nhiều hiệu quả hơn khi dùng một thuốc ở bệnh nhân có hai loại cơn mà chỉ đáp ứng với hai thuốc chống động kinh khác nhau. Có nhiều vấn đề nảy sinh khi kết hợp thuốc: tương tác dược động học, độc tính, một chế độ thuốc phức tạp, đánh giá hiệu quả và độc tính của mỗi thuốc khó khăn và cả giá thành cao hơn. Vì vậy, hai hoặc nhiều thuốc chống động kinh được sử dụng đồng thời chỉ khi sự phối hợp thuốc bảo đảm kiểm soát cơn tốt hơn mà không có nhiều tác dụng phụ hoặc cùng kiểm soát cơn với ít tác dụng phụ hơn so với dùng một thuốc.
Tính độc của các thuốc chống động kinh
Bảng 21. Tính độc của các thuốc chống động kinh
| Nhiễm độc cấp tính | Nhiễm độc mạn tính |
| Rối loạn dạ dày một | Biểu hiện (nổi mẩn, trứng cá, rám da) |
| Rối loạn chức nàng vò não | Biến đổi ờ tổ chức liên kết (tăng sản). Rối loan tự miễn (luput viêm nhiều dòng mạch, viêm tuyến giáp) |
| Rối loạn chức phận hệ thống kích hoạt lưới – vỏ | Biến đổi ở gan (tổn thương tế bào gan) |
| Rối loạn chức phận hệ thống tiểu não – tién dinh | Biến đổi chức phận thận (hội chứng thận hư) |
| Rối loạn vận động (tháp và ngoại tháp) | * Rối loạn thần kinh (bệnh não, loạn thần, biến đổi nhân cách, mất điều)
– Rối loạn nội tiết: (nhuyễn xương, chứng rậm lông (phụ nữ), tăng đường máu, biến đổi thể trọng – Bệnh bạch huyết – Phát sinh quái thai |
Nồng độ thuốc chống động kinh
Một số nghiên cứu về chỉ định
Đa số bệnh nhân sau khi uống một số liều thuốc chống động kinh sẽ đạt tới một nồng độ thuốc trong máu nhất định. Nhưng có sự khác nhau về nồng độ thuốc khi uống cùng một liều thuốc chống động kinh ở từng bệnh nhân. Điều đó cho thấy rằng kiểm soát nồng độ các thuốc chống động kinh một cách hợp lý đóng vai trò quan trọng.
Odonohoe N.v. (1994) quan niệm rằng: ngày nay sẽ là không hợp lý nếu điều trị bệnh nhân động kinh mà không kiểm soát nồng độ thuốc trong huyết tương cũng giống như sử dụng thuốc kháng đông mà không đo thời gian prothrombin, hay sử dụng thuốc điều trị tiểu đường mà lại không đo nồng độ đường trong máu.
Sự tương quan giữa nồng độ thuốc trong máu của phenytoin và độ kiểm soát cơn lần đầu tiên được chỉ ra bởi Buchtal và Svensmark (1960) và sau đó được mở rộng tới những thuốc khác. Nghiên cứu thử nghiệm và lâm sàng trong xác định nồng độ thuốc trong máu đã chỉ ra rằng đó là một số mối tương quan giữa liều thuốc và mức máu, mức máu và hiệu quả điều trị, mức máu và một số tác dụng độc.
Tuy nhiên, vai trò của định lượng nồng độ thuốc trong máu trong việc theo dõi điều trị bệnh nhân động kinh không nên được đánh giá quá cao. Những khoảng liều điều trị của các thuốc chống động kinh chỉ là một hướng dẫn tương đối cho việc xác định một liều thích hợp cho một bệnh nhân cụ thể. Mấu chốt của việc xác định vẫn là đánh giá lâm sàng về tần suất cơn động kinh và những biểu hiện của những tác dụng phụ chứ không phải là những giá trị cận lâm sàng. Một chỉ tiêu lâm sàng đáng tin cậy là có kiểm soát cơn hơn là việc quá lạm dụng trong theo dõi nồng độ thuốc.
Leppik I. (1998) đã chỉ định đo 5 lần trong một đợt điều trị trong những tình huống cụ thể sau:
Lần 1: khi một thuốc chống động kinh được bắt đầu sử dụng thì việc định lượng nồng độ thuốc trong máu sẽ giúp ích để xác định chuyển hóa của người bệnh. Ví dụ với liều phenytoin 5 mg/kg/ngày sẽ đạt được tình trạng ổn định nồng độ thuốc là 10 – 15 μg/ml. ở một vài bệnh nhân có sự thiếu hụt parahydrocylase, và vì thế có thể bị nhiễm độc ở liều này; một vài bệnh nhân chuyển hóa nhanh và đạt tới nồng độ thấp hơn. Thông tin từ lần đo này có thể ảnh hưởng đến điều chỉnh thuốc trong tương lai.
Lần 2: khi mục đích kiểm soát cơn đã đạt được, nồng độ thuốc có thể được sử dụng như là một khoảng điều trị cụ thể cho chính người bệnh.
Lần 3: để xác minh rằng người bệnh đang được tiếp tục uống thuốc như hướng dẫn. Nếu nồng độ thuốc ở dưới vùng điều trị thì những nhà lâm sàng sẽ phải lưu ý về nguy cơ tăng cơn động kinh.
Lần 4: khi bệnh nhân có cơn động kinh bất thường. Nếu nồng độ thuốc ở trong vùng điều trị thì có thể có sự thay đổi tính nhạy cảm đối với cơn động kinh hoặc là vì tiến triển xấu đi của bệnh. Nếu nồng độ dưới vùng điều trị thì có thể do tuân thủ điều trị kém hoặc dùng thêm thuốc khác mà nó làm tăng độ thanh thải của thuốc.
Tác giả đã chỉ ra rằng với độ lệch 20% hoặc ít hơn so với số trung bình của nồng độ thuốc chống động kinh là một bằng chứng cho thái độ tuân thủ đầy đủ. Giá trị giữa 20 – 45% gợi ý đến nghi ngờ lớn của việc không tuân thủ. Nếu giá trị cách xa hơn 45% chứng tỏ không tuân thủ rõ rệt.
Lần 5: khi bệnh nhân biểu hiện dấu hiệu nhiễm độc. Nồng độ thuốc có thể giúp đánh giá nguy cơ nhiễm độc, đặc biệt là những trường hợp nhẹ, nhiễm độc thần kinh tâm thần mà mọi thuốc chống động kinh đều có thể tạo ra khi dùng ở nồng độ cao (Dodrill và Troupuin, 1991). Tốt nhất là lấy được mẫu máu khi bệnh nhân nhiễm độc vì với một vài thuốc có thời gian bán hủy ngắn thì nồng độ thuốc có thể tụt thấp đến giá trị đích trong vài giờ.
Richen đã nêu ra những trường hợp đặc biệt cần phải định lượng nồng độ thuốc trong máu:
+ Tốc độ chuyển hóa biến đổi như ở trẻ em.
+ Xuất hiện hiện tượng bão hòa động học như trong sử dụng phenytoin.
+ Các chỉ số điều trị thấp trong khi liều đã gần đạt đến liều độc.
+ Các dấu hiệu nhiễm độc khó nhận ra trên lâm sàng, đặc biệt là các bệnh nhân trẻ em hoặc bệnh nhân có bệnh về thân kinh hay tâm thần.
+ Bệnh nhân sử dụng cùng một lúc nhiều loại thuốc và có dấu hiệu về tương tác thuốc.
+ Bệnh nhân có bệnh về gan, thận, hệ thống tiêu hóa và có thể ảnh hưởng đến sự hấp thu, thải trừ thuốc.
+ Nghi ngờ việc tuân thủ điều trị của bệnh nhân.
+ Động kinh kháng với thuốc điều trị.
Aldenkamp A.p. (1995), trong nghiên cứu sử dụng thuốc chống động kinh ở trẻ em đưa ra những chỉ định bô sung cho những trường hợp sau:
+ Ở giai đoạn đầu sử dụng thuốc chống động kinh để xác định nồng độ thuốc nằm trong ranh giới liều điều trị.
+ Đề phỏng đoán tăng, giảm liều phenytoin.
+ Để quyết định thuốc nào là thủ phạm nếu biểu hiện độc tố xảy ra trong sự phối hợp thuốc.
+ Vào thời điểm có trạng thái động kinh.
+ Xuất hiện cơn bất thường hoặc có thay đổi về dạng cơn trên lâm sàng.
Các phương pháp định lượng
Có nhiều cách đo nồng độ thuốc ở trong huyết tương, huyết thanh, nước bọt và các mẫu sinh học khác, sắc ký khí, sắc ký lỏng hiệu năng cao, miễn dịch huỳnh quang được sử dụng rộng rãi, đặc biệt là trong lĩnh vực nghiên cứu do tính chính xác của những phương pháp này cũng như khả năng ứng dụng rộng rãi trên các loại thuốc khác nhau. Các phương pháp trên đòi hỏi phải được thực hiện bởi các nhà hóa – sinh có kỹ năng. Miễn dịch huỳnh quang thường được sử dụng đối với các thuốc thuộc họ benzodiazepin, phương pháp này có hạn chế do sử dụng các hóa chất độc hại, đắt tiền, có tính phóng xạ cũng như đòi hỏi trang thiết bị đắt tiền, phức tạp. Phương pháp miễn dịch enzym sử dụng ái lực của các kháng thể đối với các phân tử đặc thù để định lượng một lượng nhỏ hợp chất hóa học có trong dịch sinh học.
Nguyên tắc định lượng nồng độ thuốc bằng phương pháp sắc ký khí là chiều cao hoặc diện tích đỉnh của sắc ký đồ tỷ lệ thuận với nồng độ của thuốc ở mẫu đo (A). Phương pháp miễn dịch thì có nhiều bước, nồng độ được thể hiện trên màn hình bằng các con số (B).
Lần đầu tiên ở Việt Nam, Phan Việt Nga (2002) đã nghiên cứu đo nồng độ thuốc chống động kinh trong huyết thanh của bệnh nhân động kinh.
- Đối với phenytoin:
+ Liều điều trị: 5 – 8 mg/kg/ngày cho 25 bệnh nhân động kinh.
+ Kết quả thu được: 20/25 bệnh nhân (80%) đã cắt được cơn, có nồng độ thuốc trong huyết thanh ở trong vùng điều trị vào khoảng 5 – 15 mg/ml
- Đối với natri valproat:
+ Liều điều trị: 15 – 30 mg/kg/ngày cho 17 bệnh nhân động kinh.
+ Kết quả thu được: 14/17 bệnh nhân (82,36%) đã cắt được cơn, có nồng độ thuốc trong huyết thanh ở trong vùng điều trị (50 – 100 mg/ml).
Một số yếu tố ảnh hưởng trực tiếp tới nồng độ thuốc trong máu
+ Liều sử dụng: nếu liều thấp hoặc bệnh nhân uống thuốc không đều đặn thì nồng độ thuốc trong máu sẽ thấp.
+ Sự hấp thu: công thức, kỹ thuật bào chế, dạng thuốc (dung dịch, sirô, viên nén, viên bao tan trong ruột, viên chậm, viên đặt…), kể cả những chất chứa trong dạ dày (thuốc uống trước và sau bữa ăn) ảnh hưởng trực tiếp đến sự giải phóng của dược chất vào dịch tiêu hóa. Từ đó ảnh hưởng đến tốc độ hấp thu và nồng độ của thuốc trong máu. Ngoài ra sự xuất hiện các thuốc khác và bệnh lý đường tiêu hóa cũng ảnh hưởng đến quá trình trên.
Mối liên kết của thuốc với protein huyết tương: tỷ lệ kết hợp của thuốc với protein huyết tương phụ thuộc vào bản chất lý hóa của thuốc, phụ thuộc vào tuổi và trạng thái bệnh lý của bệnh nhân và phụ thuộc vào sự xuất hiện của các thuốc khác trong cơ thể.
+ Chuyển hóa: đối với nhiều loại thuốc chống động kinh, sự đào thải phụ thuộc vào liều, nhưng đối với những thuốc đặc biệt như phenytoin, nó phụ thuộc vào enzym bão hòa (P450). Một số ngưỡng ở trên vùng điều trị, có thể xuất hiện dược động học bậc 0, dẫn tới tăng nồng độ trong huyết tương mà không liên quan tới tỷ lệ tăng liều.
+ Đào thải: sự thay đổi pH của nước tiểu hoặc suy thận có thể làm chậm sự đào thải của thuốc chống động kinh ra khỏi cơ thể.
+ Thời gian bán hủy và thời điểm của liều: sự khác nhau lớn về nồng độ trong máu của thuốc chống động kinh phụ thuộc vào thời gian bán hủy và khoảng cách sử dụng liều. Đặc biệt là đối với natri valproat.
+ Thời điểm lấy mẫu máu là quan trọng. Máu nên được lấy ở cùng thời gian liên quan đến liều. Mức cao nhất khi lấy máu từ 1 – 3 giờ sau khi uống đa sô thuốc chống động kinh (mức đinh), ngược lại để nghiên cứu nồng độ thuốc thấp nhất (mức đáy) thì lấy máu trước khi uống liều kế tiếp, thường là vào buổi sáng trước khi uống liều đầu tiên trong ngày.
Vùng điều trị
Trong điều trị, nồng độ thuốc thường được giới hạn nằm giữa nồng độ tối thiểu có tác dụng (MEC – minimum effective concentration) và nồng độ tối đa an toàn (MSC – maximum safe concentration).
Đa số bệnh nhân sẽ kiểm soát được cơn động kinh khi nồng độ thuốc chống động kinh ở trong một khoảng giới hạn, khoảng này khác nhau cho mỗi thuốc và thường được gọi là vùng điều trị (therapeutic range) có tác dụng kiểm soát cơn động kinh với ít tác dụng phụ.
Vùng điều trị là một khái niệm thống kê, thường được tính trên các nhóm bệnh nhân người lớn và khoảng điều trị này đối với trẻ em cũng thay đổi ở nhiều nghiên cứu khác nhau, nồng độ phenytoin: 5 – 15 μg/ml, 5 – 20 μg/ml, 10 – 20 μg/ml; nồng độ natri valproat: 50 – 120 μg/ml, 50 – 100 μg/ml, 40 – 150 μg/ml.
Mục đích điều trị duy nhất là cắt được cơn động kinh hay thưa cơn. Mục đích này có thể đạt được với nồng độ thuốc trong máu thấp hơn mức vùng điều trị hoặc ngược lại với nồng độ thuốc cao hơn vùng điều trị.
Nhìn chung theo nhiều tác giả, vùng điều trị đã được công bố là kết quả qua nhiều nghiên cứu thống kê nhưng không phải là căn cứ tuyệt đối để chỉnh liều cho từng bệnh nhân. Tuy nhiên, khoảng nồng độ này có thể làm cơ sở cho giai đoạn điều trị ban đầu. Khoảng liều điều trị thực sự của mỗi bệnh nhân chủ yếu căn cứ vào hiệu quả điều trị trên lâm sàng.
Trong số các thuốc chống động kinh, việc định lượng nồng độ của phenytoin trong quá trình điều trị có một vai trò đặc biệt quan trọng do đặc tính dược động học bậc 0, giới hạn điều trị hẹp và đặc biệt khi sử dụng cho trẻ em. Hoàng Kim Huyền (1996) đã nhấn mạnh rằng, với những thuốc có phạm vi điều trị hẹp, chỉ số điều trị thấp thì việc giám sát mức thuốc trong huyết thanh là rất cần thiết. Chỉ số điều trị hẹp là nồng độ cần để có tác dụng điều trị rất gần với nồng độ độc. Phenytoin là một thuốc nằm trong danh sách những thuốc cần giám sát chặt chẽ trong điều trị.


