Vai trò của điều trị hóa chất trong ung thư
Điều trị hóa chất (Chemotherapy) là phương pháp sử dụng các thuốc gây độc tế bào nhằm tiêu diệt các tế bào ác tính trong cơ thể người bệnh ung thư.
Điều trị hóa chất bắt đầu có từ những năm 1860 khi Asenitkali được sử dụng để điều trị bệnh bạch cầu, lúc đó kết quả điều trị chưa tới mức gây được sự chú ý.
Trong những năm 1940, cùng với sự phát triển của các thuốc như actinomycin, nitrogen mustard, các corticosteroid, Điều trị hóa chất đã và đang trở thành một vũ khí quan trọng trong điều trị ung thư và cấu thành một bộ phận của ngành nội khoa.
Với hơn 60 năm được sử dụng trong lâm sàng, việc áp dụng Điều trị hóa chất trong ung thư trên thế giới đã có nhiều tiến bộ đáng kể và ngày càng được nhiều nhà khoa học quan tâm, nghiên cứu. Nhiều thuốc mới được ra đời với tác dụng chống ung thư ngày càng hiệu quả và tác dụng phụ được hạn chế tới mức tối đa, cùng với nhiều phác đồ phối hợp thuốc có hiệu quả cao được xây dựng để điều trị đặc hiệu cho từng loại bệnh cụ thể và một số phác đồ trở thành kinh điển như phác đồ MOPP, ABVD trong bệnh Hodgkin, CHOP trong bệnh u lympho ác tính không Hodgkin.
Thuốc hóa chất có tác dụng chống lại hầu hết các loại ung thư. Tuy vậy mỗi loại ung thư có sự nhạy cảm với hóa chất riêng biệt. Xét một cách tổng quát, ngày nay khả năng Điều trị hóa chất ở các bệnh khác nhau được liệt kê ở bảng dưới đây:
Các bệnh ung thư hóa chất có khả năng chữa khỏi:
Bang 8: Kết quả điều trị hóa chất trên các loại ung thư
+ Bệnh bạch cẩu limphô cấp ở trẻ em
+ u limphô Burkitt
+ Ung thư nhau thai
+ Bệnh Hodgkin
+ u Wilms
+ Ung thư cơ vân thể bào thai ở trẻ em
Các loại ung thư hóa chất có khả năng kéo dài thời gian sống cho người bệnh:
+ Ung thư biểu mô tuyến vú
+ Bệnh bạch cầu limphô mãn
+ u Iimphô ác tính không Hodgkin
+ Ung thư biểu mô buồng trứng
+ Ung thư phổi tế bào nhỏ
+ u quái tinh hoàn
+ Ungthư vùng đầu-mặt-cổ
+ Bệnh bạch cầu tủy cấp
Các loại ung thư ít nhạy cảm hơn với hóa chất, hóa chất cải thiện được thời gian sống thêm cho người bệnh:
+ Saccôm xương
+ Đa u tủy
+ Ung thư phần mềm
+ Ung thư dạ dày
+ Ung thư bàng quang
+ Ung thư tuyến tiền liệt
+ Ung thư phổi không phải tế bào nhỏ
+ Ung thư đại trực tràng
Các loại ung thư rất ít nhạy cảm với hóa chất:
+ Ung thư tụy
+ Ung thư hắc tố
+ Ung thư biểu mô tế bào thận
Tuy nhiên, việc phân loại nói trên có tính tương đối. Sự phát triển không ngừng các thuốc mới với khả năng tiêu diệt tế bào u mạnh mẽ có thể làm các bệnh ít nhạy cảm với hoá chất trong thời gian này trở thành những bệnh rất nhạy cảm với thuốc trong tương lai.
Cơ chế của điều trị hóa chất
Để hiểu rõ cơ chế của Điều trị hóa chất trong ung thư, ta cần nhắc lại một số khái niệm về sự phát triển của tế bào và tác động của thuốc lên tế bào khối u sau đây:
1. Chu kỳ tế bào: gồm 4 giai đoạn hay 4 pha.
Pha S: giai đoạn tổng hợp axit nucleic.
Pha M: giai đoạn phân chia tế bào.
Pha GI và G2: các hoạt động về sinh hoá học nhưng tế bào không thay đổi về mặt hình thái học
Pha Go: tế bào không tham gia vào quá trình phân chia.
Thuốc tác dụng đến tế bào dù tế bào đang trong giai đoạn nào, kê cả giai đoạn Go được gọi là thuốc hoạt động không phụ thuộc các chu kỳ (non – cycle action drugs).
Thuốc chỉ tác dụng trên tế bào khi tế bào đang ở giai đoạn nào đó gọi là thuốc đặc hiệu cho từng giai đoạn (phase – speciíic drugs).
Thuốc chỉ có tác dụng khi tế bào đang trong chu kỳ phân chia, nhưng không đặc hiệu cho từng giai đoạn, được gọi là thuốc đặc hiệu cho chu kỳ (cycle – specific drugs).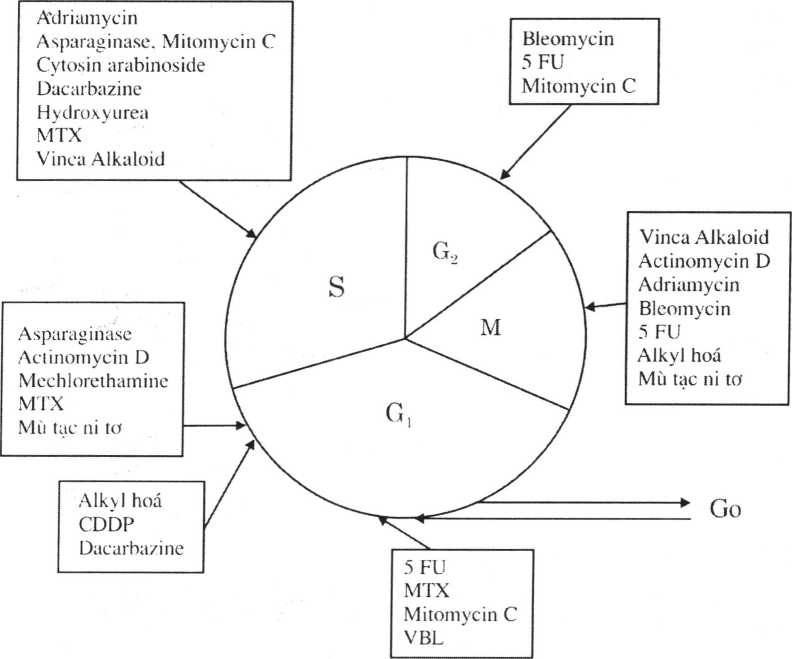
Sơ đồ 1: Thuốc hóa chất tác động theo các pha của chu kỳ tế bào.
2. Động học tế bào u
2-1. Quần thể tế bào trong khối u:
Khối u thường không thuần nhất, đựơc tạo bới hỗn hợp các tế bào ở các giai đoạn khác nhau. Có 3 nhóm được mô tả:
Các tế bào tham gia vào các giai đoạn phân chia tức là tế bào trong chu kỳ tế bào.
Các tế bào có khả năng tham gia các giai đoạn phân chia nhưng chưa phân chia tức là tế bào trong giai đoạn Go.
Các tế bào được loại ra sau mỗi chu kỳ tế bào và không thể quay trở lại chu kỳ tế bào được gọi là các tế bào chết tự nhiên.
Số lượng tế bào thuộc một trong 3 nhóm trên thay đổi tuỳ từng khối u, từng loại bệnh ung thư và từng cá thể người bệnh. Phần tế bào nằm trong chu kỳ phân chia còn được gọi là phần phát triển (growth fraction).
2-2- Thời gian nhân đôi
Thời gian nhân đôi của một ung thư là thời gian cần cho một khối u gấp đôi về số lượng tế bào. Thời gian này không giống như thời gian của một chu kỳ tế bào trừ khi phần phát triển chiếm 100% khối u. Nghiên cứu invitro cho thấy thời gian này dao động từ 15h đến 72h.
Bảng 9: Thời gian nhân đôi một số loại ung thư
| u | Thời gian nhân đôi (ngày) |
| u lympho Burkitt | 1.0 |
| Ung thư nguyên báo thai | 1,5 |
| Bạch huyết cấp thể lympho | 3-4 |
| Hodgkin | 3-4 |
| u quái tinh hoàn | 5-6 |
| ung thưvú | 60 |
| ung thư đại tràng | 80 |
| ung thư phổi không phải tế bào nhỏ | 100 |
3. Kích thước khối u:
Thành phần chính của khối u là các tế bào u. Số lượng tế bào càng nhiều, kích thước khối u càng lớn. Khi khối u lớn, việc Điều trị hóa chất bị hạn chế vì:
Một số lượng lớn các tế bào nằm trong thời kì Go.
Hệ mao mạch nuôi dưỡng u không đồng nhất, một số vùng thiếu nuôi dưỡng hoặc hoại tử, thuốc hoá chất khó vào.
Một số lượng lớn tế bào sẽ đòi hỏi phải điều trị nhiều đợt, hình thành sự kháng thuốc.
Chính vì các nguyên nhân trên, nên ở một số trường hợp như ung thư buồng trứng người ta tiến hành phẫu thuật công phá u tối đa (debulking surgery) để tạo tiền đề cho Điều trị hóa chất.
4. Thời gian điều trị
Khi đưa thuốc ở liều điều trị vào cơ thể, khối u được tiếp xúc với thuốc nhưng chỉ có một tỷ lệ nhất định tế bào u bị tiêu diệt. Việc sử dụng lặp lại liều điều trị là cần thiết để giảm tiếp số lượng tế bào u.
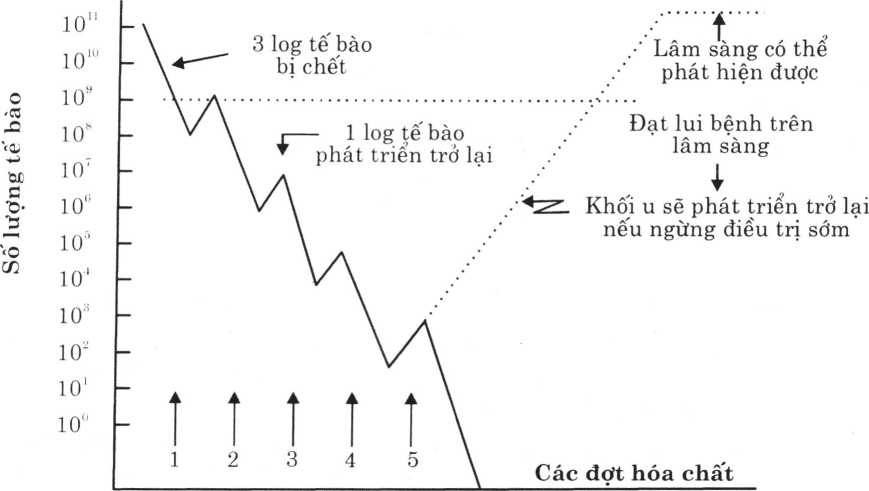
Sơ đồ 2: Mối liên quan giữa số lượng tế bào và các đợt điều trị
Qua sơ đồ trên chúng ta thấy một phác đồ điều trị có tác dụng khi số lượng tế bào ung thư bị tiêu diệt bởi hóa chất nhiều hơn số tế bào phát triển trở lại. Thời gian giữa các đợt không không nên quá xa làm cho các tế bào còn lại nhân lên với số lượng lớn. Tuy vậy, các thuốc hóa chất tác động lên cả các mô lành, cần phải có khoảng nghỉ cần thiết để cơ thể hồi phục. Số đợt điều trị (cũng là tổng thời gian của quá trình điều trị) cũng quan trọng. Nếu số đợt quá ít, các tế bào ung thư còn lại nhiều sẽ phát triển trở lại. Tuy vậy, những vấn đề về độc tính, kháng thuốc, thể trạng chung của người bệnh không cho phép chúng ta kéo dài thời gian điều trị.
5. Mối liên quan giữa tế bào u còn sống sót và liều lượng thuốc
Mối liên quan này được biểu diễn bằng công thức:
N = Noe-K (D-Do)
Trong đó:
N: Số lượng tế bào của khối u
D: Liều lượng thuốc
e: Cơ số tự nhiên
o: Chỉ liều lượng thuốc và số lượng tế bào u ban đầu
K: Số hằng định (khác nhau tuỳ loại thuốc)
Dựa vàc công thức này, sau khi tính toán ta thấy: giảm liều lượng thuốc 50%, dẫn đến tăng 98% tế bào sống sót.
Sự kháng thuốc
Sự kháng thuốc của ung thư có thể phân ra làm 2 loại:
Kháng tự nhiên: là hiện tượng không đáp ứng vốn có của loại ung thư với một thuốc nào đó.
Kháng mắc phải: là hiện tượng không đáp ứng mới phát sinh của ung thư với một thuốc nào đó mà trước đó điều trị thành công.
Có 3 nguyên nhân cơ bản gây nên sự kháng thuốc:
- Nguyên nhân về động học tế bào
Quần thể tế bào: số lượng tế bào càng lớn khả năng kháng thuốc càng cao.
Khối u phát triển ở giai đoạn đỉnh cao, phần phát triển chỉ chiếm phần nhỏ, nhiều tế bào ở thời kỳ Go sẽ ít nhạy cảm với các thuốc đặc biệt là các thuốc chống chuyển hoá.
Khối u ở vị trí không thuận lợi cho điều trị: các vị trí thuốc không tới được (nhiều thuốc không qua được hàng rào máo-não) hoặc ở xa mạch nuôi dưỡng.
- Nguyên nhân về sinh hoá
Mất khả năng chuyển hoá thuốc thành dạng có hoạt tính.
Tàng các chất trong đó có các men gây bất hoạt thuốc.
Giám khả năng đưa thuốc vào trong tế bào.
Tăng khả năng đẩy thuốc ra ngoài tế bào. Hiện tượng này có thể gây kháng một thuốc nhưng cũng có thể kháng đa thuốc sau khi tiếp xúc chỉ một loại thuốc.
- Nguyên nhân về dược động học
Giảm hoặc thay đổi hấp thu thuốc vào cơ thể.
Tăng thải trừ hoặc giáng hoá thuốc.
Tương tác với các thuốc khác.
Giảm vận chuyển thuốc tới khối u.
Độc tính của hóa chất
Đa số các thuốc hoá chất gây độc tế bào có tác dụng không đặc hiệu. Các thuốc không chỉ làm tổn hại tế bào ung thư mà còn gây tổn thương các tế bào lành đặc biệt các tế bào phân chia nhanh như tủy xương, biểu mô đường tiêu hóa. Hầu hết các phác đồ Điều trị hóa chất đều có tác dụng phụ không mong muốn. Thầy thuốc lâm sàng nên biết trước các tác dụng phụ này để phòng ngừa và kiểm soát sớm, do vậy sẽ giảm thiểu được sự mệt mỏi, suy sụp về thể chất, tinh thần của bệnh nhân hoặc các biến chứng nguy hiểm tới tính mạng người bệnh. Buồn nôn và nôn là các biểu hiện hay gặp nhất đối với độc tính của thuốc trên đường tiêu hóa. Rụng tóc là do sự tạm ngừng phát triển nang lông. Giảm bạch cầu, tiểu cầu hoặc hồng cầu do ức chế tuỷ xương. Nếu suy tuỷ nặng, bệnh nhân có thể bị nhiễm trùng, chảy máu. Việc sử dụng các thuốc chống nôn, kháng sinh, truyền máu và các sản phẩm của máu cũng như các cytokine của hệ tạo máu đóng vai trò quan trọng trong Điều trị hóa chất.
Một số thuốc có những độc tính đặc trưng như độc với tim của các anthracycline, viêm bàng quang chảy máu của cyclophosphamide và ifosfamide, bệnh thần kinh ngoại vi của các vinca alcaloid, cisplatin và paclitaxel, độc với thận của cisplatin và ifosfamide, độc với tai của cisplatin và bệnh về đông máu của L-asparaginase.
Một số thuốc có độc tính tích luỹ tức là độc tính xuất hiện sau nhiều lần dùng thuốc với tổng liều nhất định. Các thuốc anthracycline gây độc với tim, bleomycin gây độc với phổi là các ví dụ về độc tính tích luỹ.
Phân nhóm thuốc
1. Nhóm Alkyl hoá:
Là nhóm gồm nhiều thuốc có khả năng tạo các liên kết phân tử với các nucleic acid, protein và nhiều phân tử trọng lượng thấp khác. Tác dụng gây độc tế bào của các thuốc alkyl hoá là các tác dụng trên DNA với các phản ứng thay thế, phản ứng liên kết chéo hoặc các phản ứng làm gãy chuỗi. Các thông tin mã hoá trên DNA bị thay đổi dẫn đến ức chế sự sao mã hoặc sao mã không chính xác gây đột biến hoặc làm chết tế bào.
2. Chống chuyển hoá:
Để chỉ các loại thuốc có cấu trúc hoặc chức năng tương tự như các chất chuyển hoá bình thường của quá trình tổng hợp acid nucleic. Khi vào cơ thể thuốc gây ứcchế các enzym quan trọng của quá trình tổng hợp acid nucleic hoặc kết hợp vào acid nucleic tạo nên các mã sai lạc. Cả hai quá trình đều dẫn đến ức chế tổng hợp DNA và cuối cùng làm chết tế bào.
3. Các kháng sinh chống u:
Là các kháng sinh ban đầu được dùng để chống vi khuẩn nhưng về sau được phát hiện có tác dụng gây độc tế bào. Cơ chế tác dụng của các kháng sinh chống u là ức chế sự tống hợp và chức năng của các acid nucleic.
4. Các alkaloid dừa cạn:
Các thuốc trong nhóm này được chiết xuất từ cây dừa cạn (Catharanthus roscus). Thuốc tác dụng trên protein của vi quản dẫn đến giữ tế bào ớ hậu kỳ và ức chế phân bào.
5. Các taxane:
Là sản phẩm tự nhiên hoặc bán tổng hợp từ cây thông đỏ (có nơi gọi là cây thuý tùng). Các thuốc trong nhóm này có tác dụng làm ổn định quá trình polymer thành các vi quan, ứcchế sự gián phân tế bào nhưng khác với các alcaloid dừa cạn.
6. Các chất ức chế topoisomerase I:
Các thuốc có trong nhóm này có tác dụng ứcchế topoisomerase I, một men cần thiết trong quá trình tháo chuỗi DNA, tiền để cho các quá trình phiên mã và sao chép. Hiện nay, các thuốc trons nhóm này được chiết xuất từ cây Camptotheca accuminata.
7. Các chất ức chế topoisomerase II:
Các thuốc trong nhóm này là các podophvllotoxin bán tổng hợp có nguồn 2ốc từ cây Podophytỉum peỉtatum. Men topoisomerase II cũng cần thiết trong quá trình sao chép cứa DNA. Các thuốc ức chế men nàv làm gãy chuồi DNA và giữ tế bào ớ cuối pha s và dầu pha G2.
8. Men:
Asparaginase là một ví dụ về thuốc thuộc nhóm men. Men này xúc tác quá trình thủy phân asparagine trong huyết thanh thành acid aspartic và amoniac. Asparagine là acid amin cần thiết cho các tế bào bệnh bạch cầu nhưng các tế bào này không tự tổng hợp được. Các tế bào lành có thể tự tổng hợp được asparagine.
9. Các thuốc khác:
Các thuốc không xếp được nhóm và loại như muối arsen, thuốc ức chế vỏ thượng thận v.v. được liệt kê trong bảng 10.
Bảng 10: Phân loại các nhóm thuốc hoá chất
Nhóm và loại Thuốc
Alkyl hoá
| – Mù tac ni-tơ | – Mechlorethamine, chlorambucil, cỵclophosphamide, ifofamide, melphalan |
| – Dẫn chất ethỵlenimine | – Thiotepa |
| – Alkyl sulfonate | – Busulían |
| – Triazine | – Dacarbazine |
| – Nitrosourea | – Carmustine, lomustine, streptozocin |
| – Muối kim loại | – Cisplatin, carboplatin, oxalfplatin |
| Chống chuyển hoá
– Chất tương tự folic acid |
– Methotrexate |
| – Chất tương tự purine | – Mercaptopurine, thioguanine, pentostatin, cladribine, íludarabine |
| – Chất tương tự pyrimidine | – 5 Auorouracil, capecitabine, cytarabine, íloxuridine, gemcitabine |
| Các kháng sinh chống u | Bleomycin, dactinomycin, daunorubicin, doxorubicin, epirubicin, idarubicin, mitomycin, mitoxantrone |
| Alcaloid dừa cạn | – Vincristine, vinblastine, vindesine, vinorelbine |
| Các taxane | Paclitaxel, docetaxel |
| Các chất ức chế topoisomerase I | Irinotecan, topotecan |
| Các chất ức chế topoisomerase II | Etoposide, teniposide |
| Men | Asparaginase |
| Các thuốc khác
– Dẫn chất methylhydrazine |
– Procarbazine |
| – Melamine thay thế | – Altretamine |
| – Urê thay thế | – Hydroxyurea |
| – ức chế vỏ thượng thận | – Mitotane |
| – Muối arsen | – Arsenic trioxide |
| – Chất tương tự somatostatin | – Octreotide |
6. Các nguyên tắc điều trị hóa chất
Bên cạnh khả năng có thể chữa khỏi được một số loại ung thư, hóa chất có thể kéo dài thời gian sống thêm cũng như cải thiện được chất lượng sống cho người bệnh. Đa số ung thư mắc ở người có tuổi nên việc chữa trị kéo dài thời gian sống cũng rất có ý nghĩa mặc dù không loại bỏ hoàn toàn được bệnh.
Hai nguyên lý cơ bản của Điều trị hóa chất cho bệnh nhân ung thư là:
Điều trị hóa chất có thể được sử dụng rất hiệu quả để giảm các triệu chứng của bệnh nhưng độc tính của thuốc cần được lưu ý.
Luôn luôn cân nhắc mọi khía cạnh của điều trị. Bệnh nhân cần được điều trị một cách toàn diện. Trên thực tế nhiều bệnh nhân ƯT có các bệnh khác kèm theo như bệnh tim mạch, đái tháo đường, viêm phế quản mãn, viêm khớp… Thầy thuốc không chỉ quan tâm đến bệnh ung thư mà khi điều trị cần cân nhắc tới các bệnh này.
Với bất kỳ loại ung thư nào, việc Điều trị hóa chất phải được xem xét dựa trên các nguyên tắc sau đây:
1. Lựa chọn thuốc thích hợp
Cần lựa chọn các loại thuốc thích hợp nhất cho mỗi tình huống lâm sàng cụ thể. Người thầy thuốc chuyên khoa cần nắm vững được dược động học, cơ chế tác dụng, liều lượng, cách dùng, tác dụng phụ không mong muốn của thuốc. Trước khi được đưa vào sử dụng chính thức trên lâm sàng, thuốc được thử nghiệm kỹ càng trên động vật và trên các pha làm sàng.
2. Liều và liệu trình điều trị
Liều và liệu trình Điều trị hóa chất có ảnh hưởng sâu sắc đến kết quả điều trị. Mặt trái của thuốc chống ung thư là độc tính của chúng, đặc biệt tiêu diệt cả các tế bào lành đang phân chia nhanh của cơ thể. Nếu tăng liều điều trị sẽ tăng khả năng diệt tế bào ung thư nhưng nếu vượt quá mức liều “tốt nhất” thì không những không cải thiện được kết quả điều trị mà còn gây hậu quả trái ngược. Trên lâm sàng, liều thuốc được lựa chọn là liều tối đa có thể gây ra độc tính nhưng hồi phục được ở đa số bệnh nhân. Đối với các thuốc có độc tính tích luỹ, cần lưu ý tới tổng liều dùng. Các nghiên cứu thực nghiệm và lâm sàng đều cho thấy việc sử dụng hóa chất liều thấp liên tục không hiệu quả bằng điều trị liều cao ngắt quãng với khoảng thời gian thích hợp cho các tổ chức lành hồi phục. Khi điều trị liều thấp, nồng dộ thuốc sẽ không đủ cao để thâm nhập vào (vùng sâu, vùng xa) trong khối u dẫn đến hiện tượng kháng thuốc. Hơn nữa, việc điều trị như vậy sẽ không lợi dụng được sự khác nhau về động học khối u và các tổ chức lành phân chia nhanh.
Cơ sở của điều trị liều cao ngắt quãng là phá hủy một số lượng tế bào u càng nhiều càng tốt sau mỗi lần tiếp xúc với thuốc, đánh đổi bằng độc tính thoáng qua hồi phục được.
Để một khối u có thể phát hiện được trên lâm sàng, u cần phải có kích thước 109-10m tế bào. Nếu sau khi điều trị, u chỉ còn dưới 109– 1010 tế bào thì không thể phát hiện được và được coi là đáp ứng hoàn toàn. Như vậy, dù “đáp ứng hoàn toàn” cũng không đảm bảo được rằng tế bào u đã bị loại bỏ hoàn toàn. Trong thực tế, nhiều ung thư vẫn tái phát sau điều trị triệt để bởi vẫn còn một số tế bào u sống sót. Vì vậv trong một số bệnh như bệnh bạch cầu, sau khi được Điều trị hóa chất với liều mạnh “điều trị tấn công” đạt được lui bệnh hoàn toàn, người ta vẫn điều trị với phác đồ hóa chất liều thấp hơn, liệu trình thưa hơn “điều trị duy trì”. Ý nghĩa của việc làm này là kéo dài thời kỳ lui bệnh hoàn toàn và giảm thiểu các tác dụng phụ của hóa chất.
3. Phối hợp hóa chất
Cùng với tiến bộ trong phát hiện ra cơ chế của thuốc tác dụng trên tế bào, việc phối hợp các thuốc có cơ chế khác nhau có thể làm tăng kết quả điều trị. Các nghiên cứu thực nghiệm đã khẳng định giả thuyết này và đã được áp dụng trên lâm sàng. Trong một số nghiên cứu, phối hợp vincristine và prednisone để điều trị tấn công bệnh bạch cầu limphô cấp đã làm tâng ti lệ đáp ứng hoàn toàn từ 20- 30% lên 80-90%.
Phối hợp mù-tạc ni-tơ, vincristin, procarbazine và prednisone đạt được đáp ứng hoàn toàn ở 80% bệnh nhân Hodgkin trong khi dùng đơn chất chỉ đạt được lui bệnh không quá 20%. Trong hơn 40 năm qua, việc điều trị phối hợp hóa chất đã được áp dụng rộng rãi ở hầu hết các loại ung thư. Tuy nhiên, không nên cho rằng việc phối hợp thuốc luôn tạo thuận lợi trong điều trị. Một số thuốc khi phối hợp với nhau sẽ gây ra hiện tượng tranh chấp, ức chế lẫn nhau. Các nguyên tắc chung cho phối hợp hóa chất được đưa ra như sau:
Mồi thuốc trong phác đồ phối hợp đã được chứng minh có tác dụng chống ung thư khi dùng đơn thuần.
Không nên phối hợp các thuốc có cùng cơ chế tác dụng.
Các độc tính chủ yếu của các thuốc phối hợp càng khác nhau thì càng tốt.
Có một số trường hợp ngoại lệ là thêm thuốc thứ hai để giảm sự đào thải hoặc thay đổi độc tính của thuốc thứ nhất. Ví dụ: dùng acid folinic cùng với methotrexate nhằm mục đích phòng ngừa độc tính quá mức của methotrexate.
Khi sử dụng thuốc phối hợp, không phải luôn luôn tránh được độc tính chồng chéo. Vì vậy mỗi thuốc trong phác đồ điều trị phối hợp có thể có liều thấp hơn khi dùng đơn độc.
4. Phối hợp điều trị đa phương pháp
Trước đây, Điều trị hóa chất thường được sử dụng để điều trị bệnh giai đoạn muộn đã trải qua phẫu thuật và tia xạ trước đó. Sau này người ta ngày càng quan tâm nhiều đến điều trị phối hợp cả ba vũ khí trong một kế hoạch hoàn chỉnh. Trong điều trị phối hợp đa phương thức, hóa chất có vai trò hoặc để giảm thể tích u trước phẫu thuật cắt bỏ hoặc xạ trị tại chỗ, hoặc điều trị sau các phương pháp nhằm ngăn ngừa sự phát triển các vi di căn (Điều trị hóa chất bổ trợ).
Điều trị phối hợp đa phương thức được áp dụng cho nhiều bệnh. Điều trị ung thư vú là một ví dụ điển hình cho việc phối hợp hóa chất cả trước và sau điều trị tại chỗ. Các ung thư ở trẻ em như u Wilms, saccôm Ewing khi được điều trị bổ trợ bằng hóa chất kết quả cho thấy tỉ lệ sống thêm sau 5 năm, 10 năm tăng lên rõ rệt.
5. Các vị trí ẩn của tế bào ung thư
Các tế bào ung thư có thể đi cứ tới những bộ phận của cơ thể mà thuốc không thể phân bổ tới một cách hiệu quả. Các vị trí này được gọi là vị trí ẩn về dược lý học. Ví dụ bệnh bạch cầu limphô cấp, sau khi được điều trị thành công bằng hóa chất phối hợp để kiểm soát bệnh toàn thân, người ta thấy mặc dù đã đạt lui bệnh hoàn toàn và thời gian sống thêm tăng nhưng bệnh vẫn tái phát với bệnh bạch cầu màng não. Điều này được qui cho các tế bào ung thư ở hệ thần kinh trung ương đã không được tiếp xúc với các tác dụng của hóa chất đưa tới bằng đường máu. Sự trở ngại này sẽ giải quyết được bằng cách dùng thuốc trực tiếp tại vị trí ẩn đó theo đường nội tủy sống.
Methotrexate và cytosine arabinoside là các thuốc có thể dùng theo đường này và không phải tất cả các thuốc hóa chất đều có thể dùng một cách an toàn qua đường nội tủy sống. Vì vậy nếu hiện tượng ẩn trong hệ thần kinh xảy ra ở một số loại ung thư khác thì tế bào ác tính có thể thoát khỏi sự kiểm soát của thuốc.
Các vị trí ẩn khác được biết đến là tinh hoàn, các khối u lớn. Trên thực tế lâm sàng, việc cắt bỏ tinh hoàn, phẫu thuật công phá khối u “debulking surgery” trong ung thư buồng trứng là những cách loại trừ vị trí ẩn.


