VIÊM CẦU THẬN CẤP
Thường được gọi là hội chứng thận viêm. Đặc trưng bởi sự tiến triển qua nhiều ngày của tăng urê máu, tăng huyết áp, phù, đái máu, protein niệu, và thỉnh thoảng có thiểu niệu. Ứ muối và nước do giảm mức lọc cầu thận và có thể dẫn đến ứ trệ tuần hoàn. Trụ bạch cầu trong xét nghiệm nước tiểu khẳng định chẩn đoán. Protein niệu luôn <3 g/ngày.
BẢNG 152-1 NGUYÊN NHÂN CỦA VIÊM CẦU THẬN CẤP
I. Các bệnh nhiễm trùng
A. Viêm cầu thận sau nhiễm liên cầua
B. Viêm cầu thận sau nhiễm trùng không phải liên cầu
1. Vi khuẩn: viêm nội tâm mạc nhiễm khuẩn, viêm thận shunt, nhiểm khuẩn huyết, viêm phổi do phế cầu, sốt thương hàn, giang mai thứ phát, nhiễm khuẩn huyết do não mô cầu
2. Virut: viêm gan B, tăng bạch cầu đơn nhân nhiễm khuẩn, quai bị, sởi, nhiễm varicella, đậu mùa, nhiễm virut Echo, và Coxsackie
3. Ký sinh trùng: bệnh sốt rét, nhiễm Toxoplasma
II. Bệnh đa hệ thống: lupus ban đỏ hệ thống, viêm mạch, ban xuất huyết
Schönlein-Henoch, hội chứng Goodpasture
III. Bệnh cầu thận nguyên phát: viêm cầu thận màng tăng sinh typ
II, bệnh Berger (bệnh thận IgA), viêm cầu thận tăng sinh tế bào gian mạch đơn thuần
IV. Bệnh phức tạp: hội chứng Guillain-Barré, xạ trị u Wilms, tự tiêm vắc xin bạch hầu-ho gà-uốn ván, bệnh huyết thanh
aNguyên nhân hay gặp nhất.
Nguồn: RJ Glassock, BM Brenner: HPIM-13.
Hầu hết các thể của viêm cầu thận cấp đều được điều chỉnh bởi cơ chế miễn dịch dịch thể. Đặc điểm lâm sàng tùy thuộc vào tổn thương (Bảng 152-1).
Viêm cầu thận cấp sau nhiễm liên cầu
Là nguyên nhân hay gặp nhất ở trẻ em. Thận viêm tiến triển từ 1-3 tuần sau nhiễm khuẩn vùng hầu hoặc dưới da do chủng liên cầu tan huyết β nhóm A. Chẩn đoán dựa vào cấy da hoặc hầu dương tính (nếu có thể), kháng nguyên kháng liên cầu dương tính (ASO, anti-DNAse, hoặc antihyaluronidase), và giảm bổ thể máu. Sinh thiết thận cho thấy viêm cầu thận tăng sinh lan tỏa. Điều trị bao gồm điều chỉnh mất cân bằng dịch và điện giải. Bệnh tự điều chỉnh trong hầu hết trường hợp mặc dù tiên lượng không được tốt và bất thường xét nghiệm nước tiểu có nhiều khả năng tồn tại ở người lớn.
Viêm cầu thận sau nhiễm trùng
Có thể do nhiễm các loại vi khuẩn, virut và ký sinh trùng khác. Ví dụ như viêm nội tâm mạc, nhiễm khuẩn huyết, viêm gan B và viêm phổi do phế cầu. Tính chất nhẹ hơn viêm cầu thận sau nhiễm liên cầu. Kiểm soát nhiễm khuẩn ban đầu luôn làm giảm nguy cơ viêm cầu thận.
VIÊM CẦU THẬN TIẾN TRIỂN NHANH
Được định nghĩa là sự giảm bán cấp mức lọc cầu thận >50%, với bằng chứng của một viêm cầu thận tăng sinh; chồng chéo nguyên nhân với viêm cầu thận cấp (Bảng 152-2). Phân loại thành 3 dưới nhóm lớn dựa trên cơ sở của sinh thiết thận và sinh lý bệnh:
BẢNG 152-2 NGUYÊN NHÂN CỦA VIÊM CẦU THẬN TIẾN TRIỂN NHANH
I. Các bệnh nhiễm trùng
A. Viêm cầu thận sau nhiễm liên cầua
B. Viêm nội tâm mạc nhiễm khuẩn
C. Nhiễm khuẩn nội tạng thể ẩn
D. Viêm gan B nhiễm trùng (kèm viêm mạch và/hoặc cryoglobulin máu)
E. Nhiễm HIV
F. Viêm gan C (kèm cryoglobulin máu, viêm cầu thận màng tăng sinh)
II. Các bệnh hệ thống
A. Lupus ban đỏ hệ thống
B. Ban xuất huyết Schönlein-Henoch
C. Viêm mạch hoại tử toàn thân [gồm cả bệnh u hạt với viêm đa
mạch (bệnh Wegener)]
D. Hội chứng Goodpasture
E. Bệnh cryoglobulin huyết hỗn hợp (IgG/IgM)
F. Bệnh ác tính
G. Viêm đa sụn tái phát
H. Viêm khớp dạng thấp (kèm viêm mạch)
III. Thuốc
A. Penicillamin
B. Hydralazin
C. Allopurinol (với viêm mạch)
D. Rifampin
IV. Bệnh cầu thận vô căn hay nguyên phát
A. Bệnh viêm cầu thận liềm vô căn
1. Type I-lắng đọng của Ig (trung gian kháng thể kháng màng nền cầu thận)
2. Type II-lắng đọng hạt của Ig (phức hợp trung gian miễn dịch)
3. Type III-rất ít hoặc không có lắng đọng Ig (“pauci-immune”)
4. Tạo kháng thể kháng bạch cầu đa nhân, sự suy giảm của bệnh
viêm mạch
5. Viêm cầu thận Immunotactoid
6. Viêm cầu thận dạng vi sợi
B. Trên nền bệnh cầu thận nguyên phát khác
1. Bệnh viêm cầu thận màng tăng sinh (đặc biệt là typ II)
2. Viêm cầu thận màng
3. Bệnh Berger (bệnh thận IgA)
aNguyên nhân hay gặp nhất.
Nguồn: RJ Glassock, BM Brenner: HPIM-13.
(1) liên quan đến phức hợp miễn dịch, ví dụ trong bệnh lupus ban đỏ hệ thống; (2) liên quan đến không lắng đọng phức hợp miễn dịch với kháng thể kháng bạch cầu đa nhân; và (3) liên quan đến kháng thể kháng màng nền cầu thận, ví dụ trong hội chứng Goodpasture. Tất cả ba loại trên thường sẽ có một viêm cầu thận liềm tăng sinh qua soi kính hiển vi ánh sangs nhưng kết quả dưới kính hiển vi điện tử và miễn dịch huỳnh quang của sinh thiết thận là khác nhau.
Lupus ban đỏ hệ thống
Có sự tham gia của thận do lắng đọng các phức hợp miễn dịch lưu hành. Đặc điểm lâm sàng của lupus ban đỏ hệ thống có hoặc không có sự tham gia của thận gồm đau các khớp, ban hình cánh bướm, viêm thanh mạc, rụng lông tóc, và bệnh của hệ thần kinh trung ương. Hội chứng thận hư có suy thận là phổ biến. Sinh thiết thận cho thấy viêm cầu thận màng, khu trú hoặc lan tỏa và/ hoặc bệnh thận màng. Viêm cầu thận lan tỏa, kết quả hay gặp nhất của sinh thiết thận, được đặc trưng bởi một active sediment, protein niệu nặng, và suy thận tiến triển và có thể có một tiên lượng xấu. Bệnh nhân dương tính với test kháng thể kháng nhân, kháng thể kháng ADN và giảm bổ thể máu. Điều trị bao gồm Glucocorticoid và thuốc gây độc tế bào. Uống hoặc tiêm tĩnh mạch Cyclophosphamid hàng tháng là phương pháp hay được dùng nhất, đặc biệt là một lộ trình 6 tháng; bệnh nhân trong độ tuổi sinh đẻ nên gửi trứng và tinh trùng để lưu trữ. Mycophenolate mofetil là một lựa chọn.
Viêm cầu thận không lắng đọng phức hợp miễn dịch, liên quan đến kháng thể kháng bạch cầu đa nhân
Có thể giới hạn ở thận (viêm cầu thận không lắng đọng phức hợp miễn dịch vô căn) hoặc liên quan tới bệnh viêm mạch hệ thống [bệnh u hạt với viêm đa mạch (bệnh Wegener) hoặc viêm đa động mạch nút vi thể]. Đặc điểm xác đinh bệnh là sự lưu hành của kháng thể kháng bạch cầu đa nhân (ANCA). Được phát hiện bởi miễn dịch huỳnh quang của bạch cầu đa nhân cố định bằng cồn; một pANCA thường do kháng thể kháng Myeloperoxidase (MPO), trong khi một cANCA hầu như luôn luôn do phản ứng chống lại proteinase-3 (PR3). Test ELISA (enzyme-linked immunosorbent assay) kiểm tra lại kháng thể MPO và PR3 là bắt buộc, khi các pANCA có thể được tạo ra bởi kháng thể kháng các thành phần khác của bạch cầu đa nhân, ví dụ Lactoferrin; không có cùng mối liên hệ thích hợp với bệnh viêm mạc và viêm cầu thận không lắng đọng phức hợp miễn dịch. Các hiệu giá kháng thể kháng MPO và PR3 không luôn tương quan với hoạt động của bệnh.
Đặc biệt bệnh nhân có tiền triệu là hội chứng giống cúm bao gồm đau cơ, sốt, đau khớp, chán ăn, và sụt cân. Có thể liên quan tới các biến chứng dưới da, phổi, đường hô hấp trên (viêm xoang) hoặc thần kinh (viêm đơn dây thần kinh monoplex). Đặc biệt, viêm mao mạch phổi hoại tử có thể dẫn tới ho máu và xuất huyết phổi.
Điều trị chuẩn ban đầu cho viêm cầu thận tiến triển nhanh liên quan đến kháng thể kháng bạch cầu đa nhân gồm Methylprednisolon và Cyclophosphamid; đặc biệt hơn sự cạn kiệt tế bào B bởi liệu pháp kháng thể kháng CD20 với Rituximab là một lựa chọn. Một số trung tâm cũng sẽ dùng huyết tương trong điều trị ban đầu cho bệnh nhân có hội chứng thận phổi hoặc để tránh lọc máu ở bệnh nhân suy thận nặng. Steroid nhanh chóng được giảm dần liều sau khi tình trạng viêm cấp giảm; Cyclophosphamid được tiếp tục đến khi bệnh ổn định, đặc biệt trong vòng 3-6 tháng. Bệnh nhân phải đượ dự phòng viêm phổi do Pneumocystis (PCP) với Trimethoprim-sulfamethoxazol, Atovaquon, hoặc Dapson. Một vài hình thái của bảo tồn ức chế miễn dịch là tiêu chuẩn, đặc biệt từ 12-18 tháng sau khi bệnh thuyên giảm ổn định; thuốc gồm có Methotrexat, Mycophenolat mofetil, và Azathioprin.
Bệnh kháng màng đáy cầu thận
Gây nên bởi kháng thể kháng α3 NCI (không chứa collagen) là typ IV collagen; sự lưu hành kháng thể kháng màng đáy cầu thận và miễn dịch huỳnh quang tuyến tính của sinh thiết thận giúp cho chẩn đoán. Bệnh nhân có thể có viêm cầu thận khu trú; hội chứng Goodpasture trên nền viêm cầu thận và xuất huyết phổi. Thay đổi huyết tương có thể làm thuyên giảm bệnh; tiên lượng xấu với những bệnh nhân cần lọc máu hỗ trợ, với >50% tế bào hình liềm trên sinh thiết thận, hoặc creatinin >5-6 mg/dl. Xuất huyết phổi nặng được điều trị với Glucocorticoid bậc IV (1 g/ngày × 3 ngày). Xấp xỉ 10-15% sẽ có kháng thể kháng bạch cầu đa nhân chống lại MPO, một số có bằng chứng của viêm mạch, ví dụ viêm mạch máu quá mẫn trên da.
Ban xuất huyết Schönlein – Henoch
Một bệnh viêm mạch gây bệnh thận IgA, ban xuất huyết, đau khớp, và đau bụng; xảy ra chủ yếu ở trẻ em. Tổn thương thận biểu hiện bởi đái máu và protein niệu. IgA huyết thanh tăng ở phân nửa bệnh nhân. Sinh thiết thận giúp ích cho tiên lượng bệnh. Chỉ điều trị triệu chứng.
HỘI CHỨNG THẬN HƯ
Đặc trưng bởi albumin niệu (>3.5 g/ngày) và giảm albumin máu (<30g/l) và kèm theo phù, tăng mỡ máu, và lipid niệu. Bài tiết protein có thể được định lượng bằng nước tiểu 24 giờ hoặc bằng cách tính tỉ lệ protein/creatinin hoặc albumin/creatinin khi lấy nước tiểu ngẫu nhiên. Định lượng bài tiết creatinin giúp xác định sự phù hợp của nước tiểu 24 giờ: bài tiết creatinin hàng ngày nên từ 20-25 mg/kg trọng lượng cơ ở nam và 15-20 mg/kg trọng lượng cơ ở nữ. Đối với mẫu nước tiểu ngẫu nhiên, tỉ lệ protein/creatinin hay albumin/creatinin (mg/dl) xấp xỉ lượng protein bài tiết trong 24 giờ, khi bài tiết creatinin chỉ hơi lớn hơn 1000 mg/ngày/1.73 m2. Tỉ lệ protein/creatinin bằng 5 tương đương với 5 g/ngày/1.73 m2. Định lượng bài tiết protein niệu trong mẫu nước tiểu ngẫu nhiên đã thay thế phần lớn cho định lượng nước tiểu 24 giờ, do dễ dàng làm hơn và cần phải kiểm tra lại bộ nước tiểu 24 giờ hoàn chỉnh. Tỉ lệ protein toàn phần/creatinin không phát hiện được microalbumin niệu, mức độ bài tiết albumin dưới ngưỡng phát hiện của test protein toàn phần; phép đo tỉ lệ albumin/creatinin niệu được dùng nhiều hơn như một công cụ sàng lọc protein niệu mức thấp hơn.
Ngoài phù, biến chứng của hội chứng thận hư có thể kể đến như huyết khối tĩnh mạch và các biến cố huyết khối tắc mạch khác, nhiễm trùng, thiếu vitamin D, suy dinh dưỡng protein năng lượng, và ngộ đôch thuốc do giảm chất gắn với protein.
Ở người lớn, nguyên nhân thường gặp nhất của hội chứng thận hư là đái tháo đường. Một số ít trường hợp là thứ phát sau lupus ban đỏ hệ thống, bệnh thoái hóa dạng bột, do thuốc, tạo u, hoặc các rối loạn khác (Bảng 152-3).
BẢNG 152-3 NGUYÊN NHÂN CỦA HỘI CHỨNG THẬN HƯ
| Nguyên nhân hệ thống | Bệnh cầu thận |
| Đái tháo đường, lupus ban đỏ hệ thống, bệnh amyloid, bệnh thận liên quan đến HIV Thuốc: vàng, Penicillamin, Probenecid, Heroin, NSAIDs, Pamidronat, Interferon Nhiễm trùng:viêm nội tâm mạc nhiễm khuẩn, viêm gan B, nhiễm trùng qua shunt, giang mai, sốt rét, sán lá gan. Bệnh ác tính: đa u tủy, bệnh lắng đọng chuỗi nhẹ, u lympho Hodgkin và các u lympho khác, bệnh bạch cầu, ung thư biểu mô vú và đường tiêu hóa. |
Màng Thay đổi tối thiểu Xơ hóa cầu thận khu trú Cầu thận màng tăng sinh Viêm cầu thận màng tăng sinh Viêm cầu thận xơ hóa và viêm cầu thận Immunotactoid |
Nguồn: Được sử đổi bởi RJ Glassock, BM Brenner: HPIM-13.
Bằng cách loại trừ, số còn lại là vô căn. Ngoại trừ bệnh thận do đái tháo đường, sinh thiết thận là cần thiết để chẩn đoán và xác định điều trị trong hội chứng thận hư.
Bệnh thay đổi tối thiểu
Là nguyên nhân của 10-15% hội chứng thận hư vô căn ở người lớn, nhưng 70-90% hội chứng thận hư ở trẻ em. Huyết áp bình thường; mức lọc cầu thận bình thường hoặc giảm nhẹ; cặn nước tiểu là bình thường hoặc có một ít hồng cầu. Protein chọn lọc có thể thay đổi ở người lớn. Nhiễm trùng đường hô hấp trên gần đây, dị ứng, hoặc tiêm chủng có thể có trong một vài trường hợp; các thuốc chống viêm non-steroid có thể gây nên bệnh thay đổi tối thiểu với viêm kẽ thận.Suy thận cấp có thể xảy ra (hiếm), đặc biệt ở người già. Sinh thiết thận chỉ cho thấy hợp nhất chân trên kính hiể vi điện tử. Sự giảm protein niệu khi dùng Glucocorticoid mang đến một tiên lượng tốt; Liệu pháp gây độc tế bào có thể cần thiết nếu tái phát. Tiến triển đến suy thận là không thường gặp. Một vài trường hợp kháng liệu pháp steroid nghi ngờ là xơ hóa khu trú.
Viêm cầu thận màng
Được đặc trưng bởi lắng đọng IgG dưới biểu mô; chiếm tới ~30% của hội chứng thận hư vô căn ở người lớn. Bệnh nhân có phù và protein niệu trong thận hư. Huyết áp, mức lọc cầu thận và cặn nước tiểu luôn bình thường trong giai đoạn đầu. Tăng huyết áp, suy thận mức độ nhẹ, và bất thường cặn nước tiểu tiến triển muộn hơn. Huyết khối tĩnh mạch thận là tương đối phổ biến, nhiều hơn các thể khác của hội chứng thận hư. Các bệnh nền như lupus ban đỏ hệ thống, viêm gan B và các khối u rắn và tiếp xúc với các thuốc như liều cao Captopril hoặc Penicillamin nên được tìm kiếm. Phần lớn bệnh nhân viêm cầu thận màng vô căn được phát hiện có lưu hành tự kháng thể với typ M phospholipase A2 (PLA2R), được thể hiện trong tế bào có chân cầu thận.Một số bệnh nhân tiến triển tới bệnh thận giai đoạn cuối; tuy nhiên, 20-33% có thể thuyên giảm tự nhiên. Giới nam, tuổi già, tăng huyết áp và protein niệu đáng kể (>6 g/ngày) kéo dài có thể liên quan đến một nguy cơ cao của tiến triển bệnh. Điều trị ức chế miễn dịch tối ưu là một tranh cãi. Điều trị Glucocorticoid đơn độc là không hiệu quả. Thuốc gây độc tế bào có thể giúp bệnh thuyên giảm hoàn toàn hoặc một phần ở một số bệnh nhân, như là Cyclosporin. Liệu pháp kháng thể kháng CD20 với Rituximab gần đây cho thấy những hứa hẹn đáng kể, phù hợp với vai trò của tế bào B và kháng thể kháng PLA2R trong sinh lý bệnh. Làm giảm protein niệu với thuốc ức chế men chuyển và/hoặc ức chế thụ thể angiotensin cũng là một liệu pháp chính trong điều trị.
Bệnh xơ cứng cầu thận khu trú
Có thể là nguyên phát hoặc thứ phát. Bệnh nguyên phát có xu hướng cấp tính hơn, giống với bệnh thay đổi tối thiểu trong tính đột ngột của hội chứng thận hư, nhưng có thêm các đặc điểm của tăng huyết áp, suy thận và đái máu. Liên quan đến xơ cứng các phần của một vài tiểu cầu thận (chủ yếu ở gần tủy thận) và được tìm thấy trong ~35% bệnh nhân với hội chứng thận hư. Có nhiều dưới nhóm bệnh lý khác nhau của xơ cứng cầu thận khu trú vô căn có ý nghĩa tiên lượng. Đặc biệt, biến thể “bệnh cầu thận xẹp” có bệnh lý tương tự như bệnh thận liên quan đến HIV (HIVAN); tất cả đều gây nên bệnh tiến triển nhanh.
Người Mỹ gốc Phi bị ảnh hưởng rất nhiều bởi bệnh xơ cứng cầu thận khu trú, bệnh thận liên quan đến HIV và những bệnh thận không liên quan đến đái tháo đường khác, với tỷ lệ cao hơn, nhạy cảm hơn (HIVAN), và một nguy cơ cao hơn dẫn đến bệnh thận giai đoạn cuối. Những biến thể của đặc trưng của người châu Phi trong gen APOL1 – gen mã hóa apolipoprotein L1 có trong tế bào có chân cầu thận, gần đây được nhắc đến làm tăng nguy cơ di truyền.
Điều trị xơ cứng cầu thận khu trú nguyên phát bắt đầu với một đợt Steroid kéo dài; ít hơn một nửa bệnh nhân có sự thuyên giảm bệnh. Cyclosporin là một liệu pháp thay thế để bảo tồn sự thuyên giảm và cho những bệnh nhân không đáp ứng với Steroid. Cũng như trong những bệnh cầu thận khác, giảm protein niệu với thuốc ức chế men chuyển và/hoặc ức chế thụ thể angiotensin là một phần của điều trị. Cuối cùng, bệnh xơ cứng cầu thận khu trú nguyên phát có thể trở lại sau ghép thận, khi nó có thể dẫn đến mất các mô ghép cùng loài.
Bệnh xơ cứng cầu thận khu trú thứ phát có thể xảy ra ở giai đoạn muộn của bất cứ bệnh thận nào liên quan đến mất nephron (viêm cầu thận từ trước, viêm bể thận, bệnh hồng cầu hình liềm, trào ngược bàng quang-niệu đạo). Điều trị bao gồm kháng protein niệu bằng thuốc ức chế men chuyển và kiểm soát huyết áp. Glucocorticoid không có tác dụng trên bệnh xơ cứng cầu thận khu trú thứ phát. Bệnh sử, kích thước thận, kết quả sinh thiết và các điều kiện liên quan luôn cho phép phân biệt bệnh là nguyen phát hay thứ phát.
Viêm cầu thận màng tăng sinh
Mở rộng màng và tăng sinh đến tận vòng mao mạch. Hai biến thể siêu cấu trúc cùng tồn tại. Trong viêm cầu thận màng tăng sinh I, có sự lắng đọng điện tử dày đặc ở dưới nội mô, C3 lắng đọng ở các hạt liên quan đến bệnh phức hợp miễn dịch, IgG và những thành phần sớm của bổ thể có thể có hoặc không.
Ở bệnh viêm cầu thận màng tăng sinh II, lớp đặc của màng đáy cầu thận bị chuyển thành lớp dày đặc điện tử, giống như màng đáy ở bao Bowman và ống thận. C3 không thường xuyên được tìm thấy ở màng đáy cầu thận. Có mặt một số lượng nhỏ Ig (thường là IgM), nhưng những thành phần sớm của bổ thể thì vắng mặt. Nồng độ bổ thể huyết thanh giảm. Bệnh viêm cầu thận màng tăng sinh ảnh hưởng tới người trẻ trưởng thành. Bất thường huyết áp và mức lọc cầu thận, và cặn nước tiểu hoạt động. Một số có viêm thận cấp hoặc đái máu. Tổn thương giống nhau ở lupus ban đỏ hệ thống và hội chứng tan máu urê máu. Nhiễm trùng với viêm gan V có liên kết với viêm cầu thận màng tăng sinh, thường liên quan đến bệnh cryoglobulin huyết. Điều trị với Interferon α và Ribavirin có hiệu quả trong làm thuyên giảm bệnh thận ở một số trường hợp, tùy thuộc vào typ huyết thanh vủa viêm gan C; tuy nhiên, suy thận đặc biệt không đáp ứng với liệu pháp Ribavirin. Glucocorticoid, thuốc gây độc tế bào, chống kết tập tiểu cầu và liệu pháp huyết tương tinh chế được sử dụng với độ thành công hạn chế; Rituximab là một liệu pháp mới với các bằng chứng có lợi nhiều hơn. Viêm cầu thận màng tăng sinh có thể tái phát khi ghép mô cùng loài.
Bệnh thận do đái tháo đường
Là nguyên nhân hay gặp nhất của hội chứng thận hư. Dù giai đoạn trước của đái tháo đường có thể thay đổi, ở typ 1 protein niệu có thể tăng sau 10- 15 năm từ khi phát bệnh, tiến triển tới hội chứng thận hư và sau đó đến suy thận sau 3-5 năm. Bệnh võng mạc gần như phổ biến ở bệnh nhân đái tháo đường typ 1 có bệnh thận, vì vậy sự vắng mặt của bệnh võng mạc cần xem lại tổn thương cầu thận khác (bệnh thận màng). Ngược lại, chỉ ~60% bệnh nhân bệnh thận do đái tháo đường typ 2 có bệnh võng mạc. Đặc điểm lâm sàng gồm protein niệu, tăng huyết áp tiến triển và suy thận tiến triển. Thay đổi bệnh lý bao gồm xơ cứng màng, lan tỏa, và/hoặc xơ cứng cầu thận dạng nốt (Kimmelstiel-Wilson). Tuy nhiên, bệnh nhân hiếm khi làm sinh thiết thận; tới mức mà định lượng microalbumin niệu hàng năm là cách quản lý thường xuyên cho tất cả bệnh nhân đái tháo đường, bệnh sử tự nhiên là một phần quan trọng của chẩn đoán. Sự tiến triển từ microalbumin niệu (30-300 mg/24 giờ) đến que thử dương tính (>300 mg albumin niệu) và sau đó tiến đến rõ ràng và bệnh thận mạn. Tuy nhiên, protein niệu có thể khá thay đổi ở bệnh thận do đái tháo đường, nhiều như 25 g/24 giờ khi không có suy thận nặng hoặc giá trị khác với suy thận tiến triển và ổn định, protein niệu vừa phải.
Điều trị với thuốc ức chế men chuyển trì hoãn khởi phát của bệnh thận nói chung và bệnh thận gia đoạn cuối nói riêng ở bệnh nhân đái tháo đường typ 1 với microalbumin niệu và/hoặc giảm chức năng thận và nên được áp dụng cho mọi bệnh nhân không có chống chỉ định. Nếu có ho ở bệnh nhân điều trị ức chế men chuyển, một thuốc ức chế thụ thể angiotensin là lựa chọn tốt tiếp theo. Đái tháo đường typ 2 với microalbumin niệu hoặc protein niệu có thể được điều trị với ức chế men chuyển hoặc ức chế thụ thể angiotensin. Dù thiếu các nghiên cứu dài hạn, nhiều tác giả ủng hộ ức chế tổng hợp của hệ thống renin-angiotensin-aldosterone (RAAS), ví dụ ức chế thụ thể angiotensin, ức chế men chuyển, chẹn thụ thể mineralocorticoid, và/hoặc ức chế renin, dấu hiệu của bệnh dai dẳng là protein niệu. Tăng kali máu, tụt huyết áp, và/ hoặc mức lọc cầu thận càng tồi tệ hơn có thể giới hạn điều trị đơn độc hoặc kết hợp với ức chế RAAS. Nếu tăng kali máu tiến triển và không thể kiểm soát với (1) tối ưu hóa kiểm soát đường huyết, (2) lợi tiểu quai (nếu những liệu pháp khác không hiệu quả), hoặc (3) điều trị nhiễm toan chuyển hóa (nếu có), sau đó kiểm soát huyết áp chặt chẽ với các thuốc thay thế được bảo đảm. Sự lượng giá hội chứng thận hư được nêu ở Bảng 152-4.
BẢNG 152-4 LƯỢNG GIÁ HỘI CHỨNG THẬN HƯ
Mẫu nước tiểu ngẫu nhiên cho protein và creatinin
Albumin, cholesterol, bổ thể huyết thanh
Điện di protein nước tiểu
Loại trừ bệnh lupus ban đỏ hệ thống, đái tháo đường
Xem lại thuốc đã dùng
Sinh thiết thận
Xem xét bệnh ác tính (ở người già với viêm cầu thận màng hoặc bệnh thay đổi tối thiểu)
Xem xét huyết khối tĩnh mạch thận (nếu có viêm cầu thận màng hoặc có triệu chứng của thuyên tắc phổi)
BẢNG 152-5 NGUYÊN NHÂN CẦU THẬN CỦA BẤT THƯỜNG KHÔNG TRIỆU CHỨNG HỆ TIẾT NIỆU
I. Đái máu có hoặc không protein niệu
A. Các bệnh cầu thận nguyên phát
1. Bệnh Berger (Bệnh thận IgA)a
2. Viêm cầu thận màng tăng sinh
3. Đái máu do bệnh cầu thận nguyên phát khác đi kèm tăng sinh màng đơn thuần, viêm cầu thận tăng sinh khu trú và từng đoạn, hoặc các tổn thương khác.
4. Bệnh màng đáy mỏng (hình thái không điển hình của hội chứng Alport)
B. Liên quan đến bệnh hệ thống hoặc bệnh di truyền
1. Hội chứng Alport và bệnh đái máu lành tính có tính chất gia đình
2. Bệnh Fabry
3. Bệnh hồng cầu hình liềm
C. Liên quan đến nhiễm trùng
1. Viêm cầu thận sau nhiễm liên cầu đang thoái triển
2. Viêm cầu thận sau nhiễm trùng khác
II. Protein niệu không chỉ do thận hư
A. Các bệnh cầu thận nguyên phát
1. Albumin niệu thế đứng
2. Xơ cứng cầu thận khu trú và từng đoạn
3. Viêm cầu thận màng
B. Liên quan đến bệnh hệ thống hoặc bệnh di truyền
1. Đái tháo đường
2. Bệnh Amyloid
3. Hội chứng Nail-patella
aHay gặp nhất.
Nguồn: RJ Glassock, BM Brenner: HPIM-13.
BẢNG 152-6 KẾT QUẢ XÉT NGHIỆM HUYẾT THANH TRONG BỆNH HỆ THỐNG GÂY BỆNH CẦU THẬN
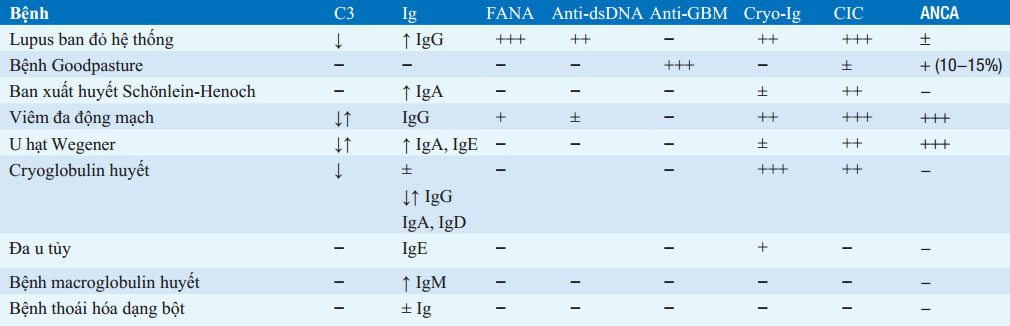
Các từ viết tắt: ANCA: kháng thể kháng bạch cầu đa nhân; anti-dsDNA: kháng thể kháng ADN; anti-GBM: kháng thể kháng màng đáy cầu thận; CIC: phức hợp miễn dịch lưu hành; cryo-Ig, tủa lạnh globulin miễn dịch; C3: thành phần bổ thể 3; FANA: xét nghiệm tìm kháng thể kháng nhân bằng huỳnh quang; Ig: globulin miễn dịch ; −: bình thường ; +: thỉnh thoảng có bất thường nhẹ; ++: thường bất thường ; +++: bất thường nặng.
BẤT THƯỜNG KHÔNG TRIỆU CHỨNG CỦA HỆ TIẾT NIỆU
Protein niệu trong khoảng không phải thận hư và/hoặc đái máu không kèm theo phù, giảm mức lọc cầu thận, hoặc tăng huyết áp có thể do nhiều nguyên nhân (Table 152-5).
Bệnh cầu thận màng đáy mỏng
Được biết là một bệnh đái máu di truyền lành tính, có thể gây đến 25% của đái máu dai dẳng không có protein niệu. Trên sinh thiết thận thấy màng đáy cầu thận mỏng lan tỏa với những thay đổi tối thiểu khác. Có thể di truyền, trong một số trường hợp gây nên bởi thiếu collagen typ IV. Bệnh nhân có đái máu do cầu thận dai dẳng với protein niệu lượng rất nhỏ. Tiên lượng đang còn tranh cãi nhưng tương đối lành tính.
Bệnh thận IgA
Là một nguyên nhân thường gặp nữa của đái máu tái phát ở bệnh cầu thận; hay xảy ra ở người trẻ tuổi. Biểu hiện của đái máu đại thể gồm triệu chứng giống cúm, không nổi ban da, đau bụng hoặc viêm khớp. Sinh thiết thận cho thấy lắng đọng IgA lan tỏa màng thận, thường có rất ít IgG, gần như luôn bằng C3 và properdin nhưng không bằng C1q hay C4. Tiên lương có thể thay đổi; 50% tiến đến bệnh thận giai đoạn cuối trong vòng 25 năm; bệnh nhân có tăng huyết áp và protein niệu nặng có nguy cơ cao hơn. Glucocorticoid và các chất ức chế miễn dịch khác không tỏ ra hiệu quả, trừ những bệnh nhân có viêm cầu thận tiến triển nhanh. Một thử nghiệm lâm sàng ngẫu nhiên bổ sung dầu cá cho thấy lợi ích trị liệu không cao. Hiếm khi tái phát khi ghép mô cùng loài.
Các bệnh cầu thận liên quan đến bệnh hệ thống (Bảng152-6)


